مقاومت الکتریکی
مقاومت الکتریکی یک مقاومت ایدهال عنصری است با یک مقاومت الکتریکی که صرفنظر از ولتاژ اعمالی به دو سرش یا جریان الکتریکی عبوری از آن ، ثابت میماند. اما بدلیل اینکه مقاومتهای جهان واقعی نمیتوانند این شرایط ایدهال را برآورده سازند، آنها را بگونهای طراحی میکنند که در برابر تغییرات دما و دیگر عوامل محیطی ، نوسانات کمی در مقاومت الکتریکی شان ایجاد شود. مقاومتها ممکن است که ثابت یا متغییر باشند. مقاومتهای متغیر پتانسیومتر یا رئوستا نیز خوانده میشوند و این اجازه را میدهند که مقاومت وسیله توسط تنظیم یک میله یا لغزش یک ابزار کنترلی ، تغییر کند.
برخی از مقاومتها بلند و نازک هستند و ماده مقاوم حقیقی در وسط آنها قرار دارد و یک پایه هادی در هر انتهای آن نصب شده است. به این مقاومت بسته محوری گفته میشود. تصویر سمت راست یک ردیف از مقاومتهایی را نشان میدهد که عموما در یک بسته بندی قرار داده میشوند. مقاومتهای استفاده شده در کامپیوترها و دیگر وسایل ، نوعا خیلی کوچکتراند و اغلب در بستههای با پایه سطحی (فن آوری پایه سطحی) بدون سیمهای رابط بکار میروند. مقاومتهای با توان بالاتر را در بستههای محکمتری قرار میدهند و بگونهای طراحی شدهاند که گرما را بطور موثری از بین ببرند، اما تمامی آنها دارای همان ساختار قبلی مقاومتها هستند.
مقاومتها به عنوان بخشی از شبکههای الکتریکی بکار میروند و در علم میکرو الکترونیک و ابزارهای نیمه هادی شرکت دارند. اندازه گیری دقیق یک مقاومت بصورت نسبت ولتاژ به جریان است و واحد آن در دستگاه SI، اهم است. یک عنصر دارای مقاومت 1 اهم است اگر یک ولتاژ 1 ولتی دو سر عنصر منجر به یک جریان 1 آمپر شود که معادل جریان یک کولمب بار الکتریکی (تقریبا 6.242506 X 10 18 الکترون) در ثانیه در جهت مخالف است.
یک جسم فیزیکی نوعی مقاومت است. اکثر فلزات، مواد هادی هستند و در برابر جریان الکتریسته مقاومت کمی دارند. بدن انسان ، یک تکه پلاستیک ، یا حتی یک خلا دارای مقاومتهایی هستند که قابل اندازه گیری است. موادی که دارای مقاومتهای بسیار بالایی هستند عایق نامیده میشوند.
رابطه بین ولتاژ ، جریان و مقاومت در یک جسم توسط یک معادله ساده که از قانون اهم گرفته شده و اغلب با آن اشتباه میشود، بیان میشود:
که در آن V ولتاژ دو سر مقاومت بر حسب ولت ، I جریان عبور کننده از مقاومت بر حسب آمپر و R مقدار مقاومت بر حسب اهم است. اگر V و I دارای یک رابطه خطی باشند که به مفهوم ثابت بودن R در یک محدوده است، آنگاه این ماده در آن محدوده اهمی خوانده میشود. یک مقاومت ایده آل دارای مقاومت ثابت در تمامی فرکانسها و مقادیر ولتاژ و جریان است. مواد ابر رسانا در دماهای بسیار پایین دارای مقاومت صفر هستند. عایقها ( نظیر آزمایشهای مربوط به هوا ، الماس ، یا مواد غیر هادی) ممکن است دارای مقاومتهایی بسیار بالا (اما نه بینهایت) باشند. لکن تحت ولتاژهای به میزان کافی زیاد، دچار شکست می شوند و جریان بزرگی را از خود عبور میدهند.
مقاومت یک عنصر را میتوان از مشخصههای فیزیکی آن محاسبه کرد. مقاومت با طول عنصر و مقاومت ویژه (یک خاصیت فیزیکی ماده) آن بطور مستقیم متناسب است و با سطح مقطع آن رابطه عکس دارد. معادله محاسبه مقاومت یک بخش ماده مانند زیر است:
که در آن r مقاومت ویژه ماده ، L طول و A مساحت سطح مقطع است. این معادله را میتوان برای موادی که از نظر شکل پیچیدهترند، بصورت انتگرالی نیز نوشت. اما این فرمول ساده برای سیمهای استوانهای و اغلب هادیهای عمومی قابل استفاده است. این مقدار میتواند در فرکانسهای بالا به علت اثر پوستی ، که سطح مقطع در دسترس را کاهش میدهد، تغییر کند. مقاومتهای استاندارد را در مقادیری از چند میلی اهم تا حدود یک گیگا اهم به فروش میرسانند. تنها محدوده مشخصی از مقادیر که مقادیر ترجیح داده شده نام دارند در دسترس هستند.
در عمل ، اجزای گسسته فروخته شده به عنوان مقاومت ، یک مقاومت کامل آنگونه که در بالا تعریف شد، نیستند. مقاومتها معمولا توسط خطایشان (حداکثر تغییرات مورد انتظار نسبت به مقاومت مشخص شده) بیان میشوند.
در یک مقاومت با رنگ کد گذاری شده باند منتهی الیه سمت راست. اگر به رنگ نقرهای باشد خطای 10 درصد ، اگر به رنگ طلایی باشد خطای 5 درصد ، اگر به رنگ قرمز باشد خطای 2 درصد و اگر به رنگ قهوهای باشد خطای 1 درصد را نشان میدهد. مقاومتهای با خطای کمتر هم وجود دارند که مقاومتهای دقیق خوانده میشوند.
یک مقاومت دارای حداکثر ولتاژ و جریانی است که فراتر از آنها ، مقاومت ممکن است تغییر کند (در بعضی موارد به شدت) یا از نظر فیزیکی از بین برود (برای مثال بسوزد). اگر چه که برخی از مقاومتها دارای ولتاژ و جریان نامیاند، اغلب آنها توسط یک توان فیزیکی حداکثر که توسط اندازه فیزیکی تعیین میشود، ارزیابی میشوند. عموما توان نامی برای مقاومتهای کامپوزیت کربن و مقاومتهای ورقه فلزی 1.8 وات ، 1.4 وات و 1.2 وات است. مقاومتهای ورق فلزی نسبت به مقاومتهای کربنی در برابر تغییرات دما و گذر زمان پایدارترند.
مقاومتهای بزرگتر قادرند که گرمای بیشتری را بدلیل سطح وسیعترشان از بین ببرند. مقاومتهای سیم پیچی شده و پر شده با شن هنگامی بکار میروند که توان نامی بالاتری مانند 20 وات مورد نیاز باشد. بعلاوه تمامی مقاومتهای حقیقی کمی خواص سلفی و خازنی از خود نشان میدهند که رفتار دینامیکی مقاومت ، ناشی از معادله ایده آل آن را تغییر میدهد.
هر کدام از مقاومتهای یک ساختار مداری سری و موازی دارای اختلاف پتانسیل (ولتاژ) یکسان هستند. برای محاسبه مقاومت معادل کل آنها:
خاصیت موازی بودن را میتوان برای ساده سازی معادله ، با دو خط موازی (مانند هندسه) در معادلات نمایش داد. برای دو مقاومت موازی داریم:
جریان هر مقاومت در مدارهای سری و موازی ثابت است، اما ولتاژ در طول هر مقاومت ممکن است متفاوت باشد. مجموع اختلاف پتانسیلها (ولتاژ) برابر ولتاژ کلی است. برای محاسبه مقاومت کلی آنها:
یک شبکه مقاومتی که ترکیبی از مدارهای سری و موازی است را میتوان به اجزا کوچکتری تجزیه کرد که یکسان یا غیر یکسانند. برای مثال:
مقاومت متغیر مقاومتی است که مقدارش میتواند توسط یک حرکت مکانیکی تعیین شود، برای مثال توسط دست تنظیم شود. مقاومتهای متغیر میتوانند از نوع ارزان و تک دور یا از نوع چند دور با یک عنصر مارپیچی باشند. برخی از آنها حتی دارای نمایشگر مکانیکی تعداد دور نیز هستند. بطور سنتی مقاومتهای متغیر نامطمئن بودهاند، چرا که سیم یا فلز خورده یا فرسوده میشوند. (یک روش دیگر کنترل که در واقع یک مقاومت نیست اما شبیه آن عمل میکند، شامل یک سیستم سنسور فتو الکتریک است که چگالی نوری یک ورقه را اندازه میگیرد. بدلیل اینکه سنسور ورقه را لمس نمیکند، پوسیدگی رخ نمیدهد.)
یک پتانسیومتر نوعی از مقاومتهای متغییر است که بسیار عام است. یکی از استفادههای عمومی آن به عنوان کنترل صدا در تقویت کنندههای صوتی است. یک واریستور اکسید فلزی ، یا MOV نوع بخصوصی از مقاومت است که دارای دو مقدار مقاومت بسیارمتفاوت است، یک مقاومت بسیار بالا در ولتاژ پایین (زیر ولتاژ راه انداز) و یک مقاومت بسیار کم در ولتاژ بالا (بالاتر از ولتاژ راه انداز). این نوع از مقاومت معمولا برای حفاظت اتصال کوتاه در برقگیر تیر برق خیابانها یا به عنوان یک اسنابر استفاده میشود. یک مقاومت با ضریب دمایی مثبت/PTC یک مقاومت وابسته به دما است که دارای یک ضریب دمایی مثبت است.
وقتی که دما افزایش مییابد، مقاومت هم زیاد میشود. PTC ها اغلب در تلویزیونها بصورت سری با سیم پیچ دمغناطیس کننده یافت میشوند که یک جرقه جریان کوتاه را از طریق سیم پیچ در هنگام روشن کردن تلویزیون ایجاد میکند. یک نسخه تخصصی یک PTC چند سوییچ است که مانند یک فیوز خود تعمیر عمل میکند. یک مقاومت با ضریب دمایی منفی/NTC نیز یک مقاومت وابسته به دماست، اما دارای یک ضریب دمایی منفی است. وقتی که دما افزایش مییابد مقاومت NTC کاهش مییابد. NTC ها عموما در آشکار سازهای دمای ساده و در ابزارهای اندازه گیری بکار میروند.
| | نسخه قابل چاپ | تعداد بازديد : 49 |


آهنربا از دو بخش آهن و -ربا از فعل ربودن تشکیل شده. کاربرد واژههایی مانند آهنربا و کهربادر فارسی پیشینه طولانی دارد.
برابر اروپایی آن: اولین شرح مغناطش به یونانیان قدیم باز میگردد که این اسم را به مغناطیس دادند. این اسم از مگنزیا که نام یک دهکدهٔ یونانی است، مشتق شدهاست. از لحاظ لغوی Magnet به معنی «سنگی از اکسید آهن» است. این سنگ حاوی مگنتیت (Fe3O4) بود و هنگام مالش آن به آهن، آن را آهنربا میکرد. نظریهٔ دیگر این است که این واژه از ریشهٔ واژهٔ فارسی «مگ» میباشد و این واژه magnet به همراه واژهٔ magic از ریشهٔ واژهٔ پارسی mag میباشند، که خود برگرفته از مغان ایران است.
جدی برای استفاده از قدرت پنهان مواد مغناطیسی بسیار پس از کشف آن انجام شد. به عنوان مثال در قرن ۱۸ام با ادغام تکههای کوچک مواد مغناطیسی تکهٔ بزرگتری بدست آمد که مشخص شد توانایی بلند کردن قابل توجهی دارد.
پس از اینکه اورستد در سال ۱۸۲۰ کشف کرد که جریان الکتریکی میتواند میدان مغناطیسی به وجود آورد، پیشرفتهای زیادی در این زمینه حاصل شد.
استورگن دانش خودش را با موفقیت برای ساخت اولین آهنربای الکتریکی در سال ۱۸۲۵ بکار برد. با اینکه دانشمندان زیادی (از قبیل گاوس، ماکسول و فارادی) با این پدیده از دیدگاه تئوریک درگیر شدند، اما توصیف درست مواد مغناطیسی به فیزیکدانان قرن بیستم نسبت داده میشود.
کیوری و ویس در شفافسازی پدیدهٔ مغناطش دائمی و وابستگی دمایی آن موفق بودند. ویس فرضیهٔ وجود حوزههای مغناطیسی را مطرح کرد تا توضیح دهد که مواد چگونه میتوانند آهنربا شده یا خاصیت مغناطیسی کل آنها صفر شود.جزئیات خواص دیوارههای این حوزههای مغناطیسی توسط بلوچ، لاندو و نیل بررسی شد
آهنرباهای دائم از صخرههای طبیعی به نام لودستون بدست آمدند. این سنگها برای اولین بار،۲۵۰۰ سال پیش توسط چینیها و سپس توسط یونانیها مطالعه شدند. یونانیها اولین بار آهنربا را از منطقهٔ Magnetes بدست آوردند که امروزه آهنرباها به این نام، شناخته میشوند. از آن دوران تا به امروز، خواص مواد مغناطیسی بهینه شده و آهنرباهای دائم امروزی صدها برابر قویتر از آهنرباهای پیشین هستند.
امروزه چهار خانوادهٔ بزرگ از مواد مغناطیسی دائم، بطور تجاری کاربرد دارند. این مواد از فریتها که انرژی پایینی دارند تا آهنرباهای خاکی نادرکه انرژی بالایی دارند، متغیرند. دمای کارکرد، محدودیت اندازه و وزن، مسائل زیست محیطی و انرژی مغناطیسی از جمله عواملی است که بر انتخاب یک مادهٔ مغناطیسی تاثیر میگذارند

آهنربای دائم به اختصار PM1 خوانده میشود و قطعهای از فولاد سخت و یا دیگر مواد مغناطیسی که تحت اثر میدانهای شدید ، مغناطیس شده و این اثر را برای مدت طولانی در خود حفظ میکنند. اثر آهنربایی اولین بار ، روی قطعههایی از سنگ معدن آهن ، به نام آهنربای طبیعی یا معدنی در طبیعت مشاهده شد و دیدند که قطعات آهن را به خود جذب میکند.
بعدا دریافتند که چنانچه قطعه درازی از این سنگ آهن مغناطیسی معدن را ، بطور معلق در هوا نگهدارند این قطعه دراز خود را در امتدادی قرار میدهد که یک انتهایش به طرف قطب شمال زمین قرار دارد و این انتهای میله آهن مغناطیس دار را قطب شمال و سر دیگر آن را قطب جنوب نامیدند. چنین قطعه سنگ معدن آهن ، آهنربای میلهای نامیده شد.
نظریه اول آهنربایی
هر آهنربا از تعدادی ذره آهنربایی تشکیل شده است. وقتی یک قطعه آهن ، آهنربا نیست، ذرات آهنربایی بطور پراکنده و دلخواه داخل آن قرار دارند و وقتی ذرات داخل آهن در امتدادی منظم قرار گیرند، اثرات مغناطیسی آنها باهم جمع شده و آن آهن ، آهنربا میشود.
نظریه دوم آهنربایی
خاصیت آهنربایی به الکترونها وابسته است. الکترون دارای یک نیروی دوار در اطراف خود میباشد و وقتی مدارهای الکترونها در امتداد میله آهن طوری قرار گیرند که دایرههای نیرو با یکدیگر جمع شوند، میله آهنی ، آهنربا میشود. در طبیعت از نقطه نظر تغییرات چگالی فلوی مغناطیسی (B) بر حسب جریان (I) میتوان مواد را به دو دسته تقسیم نمود:
1. مواد غیر مغناطیسی: از این مواد میتوان پلاستیک و میکا و عایقهای جریان الکتریکی را نام برد. در این مواد ، نفوذ پذیری مغناطیسی عددی ثابت است و مقدار آن را µ˚= 4π×10-7 فرض میکنیم.
2. مواد مغناطیسی: مواد مغناطیسی که به مواد فرومغناطیسی نیز معروفند جزء گروه آهن به شمار میروند. در این مواد با جریان مفروض I چگالی شار (B) افزونتری نسبت به فضای آزاد شکل میگیرد و منحنی B-I این مواد غیر خطی است. مواد مغناطیسی خود به دو گروه تقسیم بندی میشوند:
• مواد فرومغناطیسی نرم: که آنها خطی کردن تغییرات B بر حسب I (منحنی B-I) امکان پذیر است، از تقریب خوبی برخوردار میباشد و در این مواد ، B بخاطر I حاصل میشود.
• مواد فرومغناطیسی سخت: که از اینگونه مواد برای ساخت مغناطیس دائم استفاده میشود. در این مواد B بخاطر دو عامل جریان (I) و خاصیت مغناطیس شوندگی ماده (M) بروزمی کند. این مواد در اثر میدانهای شدید ، مغناطیس شده و این اثر را تا مدت طولانی خود حفظ میکنند.
مواد مغناطیسی برای مقاصد خاص نیز ساخته میشوند، بطوری که طی سی سال گذشته چند ماده مغناطیسی جدید ساخته شده که مشخصات لازم برای ایجاد یک آهنربای دائم خوب را دارا هستند. آهنربای دائم خوب ، از مادهای است که تا حد امکان شار باقیمانده (یا چگالی شار باقیمانده) بزرگی داشته باشند. عمده این مواد فریتها (مواد مغناطیسی سرامیکی) و مواد مغناطیسی خاک کمیاب هستند.
انواع آهنربای دائم
سه نوع آهنربای دائم که دارای کاربرد فراوان هستند به شرح زیرند:
آهنربای آلنیکو
آلنیکو از ابتدای نام سه عنصر آلومینیوم ، نیکل و کبالت گرفته شده است. این آلیاژ که عمدتا از فلزات آهن و آلومینیوم و نیکل و کبالت ساخته میشود، قابلیت پذیرش نیروی مغناطیسی بالایی و به منظور ساختن آهنربای دائم بلندگوها و لامپهایی با حوزه مغناطیسی و در سروموتورهای DC2 پیشرفته استفاده میشود.
معمولا در آخر اسم "آلنیکو" حرفی اضافه میگردد که مشخص کننده قدرت آهنربا است. فرضا "آلنیکوv" قویترین آهنربای دائم نسبت به "آلنیکوها" است و معمولا آهنربای "آلنیکو" را به صورت طولی مغناطیس میکنند و سپس مورد استفاده قرار میدهند. منظور از مغناطیس کردن طولی این است که دو قطب S و N در طول جسم قرار میگیرند.
آهنربای فریت
این آهنربا را آهنربای سرامیک نیز مینامند. این آهنربای دائم از ترکیب مواد ذوب شده نوعی چینی و پودر ماده مغناطیسی ساخته میشود. این آهنربا چون پودر پس ماند مغناطیسی و نیروی خنثی کننده زیادی دارد، آن را به صورت عرضی مغناطیسی میکنند. منظور از مغناطیس کردن عرضی ، قرار گرفتن دو قطب S و N در عرض جسم است و چون چگالی شار (B) این آهنربای دائم کم است برای جبران چگالی شار زیاد، آن را دراز می سازند.
چون هزینه ساخت این آهنربا کم بوده و مواد اولیه آن به ارزانی قابل تهیه است، بطور گسترده مورد استفاده قرار میگیرد. نامگذاری آهنربای فریت با توجه به نوع عنصری که در ساخت آهنربا از آن استفاده شده است صورت میگیرد. مثل فریت استرونیتام و یا فریت باریم.
آ هنربای سارماریوم - کبالت
عنصر اصلی این آهنربای دائم عنصر ساماریوم با علامت اختصاری Sm و عدد اتمی 62 است. چون این آهنربای کمیاب (به دلیل عنصر تشکیل دهنده کمیاب ساماریوم) دارای پس ماند مغناطیسی و خنثی کننده خیلی زیادی است، به همین دلیل میتواند شدتی به مراتب بزرگتر از آهنربای دائم معمولی داشته باشد. به عنوان مثال در یک طول و مساحت برابر ، چگالی شار (B) این آهنربا دو برابر آهنربای سرامیک است.
هزینه تولید این آهنربا قابل ملاحظه است و به همین دلیل آن را کم قطر میسازند. چون شدت مغناطیسی این آهنربا بالا است، لذا از چنین آهنربایی که در ابعاد کوچک و وزن کمتر شدت مغناطیسی خوبی دارد در ساعتهای الکترونیکی و لامپهای ماگنترون و تجهیزات نظامی و سروموتورها هواپیما استفاده میکنند. به این ترتیب روز به روز دامنه کاربرد این آهنربا رو به افزایش است.
آ هنربای الکتریکی با نیروی بالا برندگی زیاد :
برای بدست آوردن آهنربای الکتریکی با نیروی بالا برنده تا حد امکان زیاد ، باید سطح تماس بین قطبهای آهنربا و جسم آهنی جذب شده (معروف به جوشن) را افزایش داد، و سعی کرد تا تمام خطوط میدان مغناطیسی فقط از آهن بگذرد، یعنی تمام فواصل هوا یا شکافهای بین جوشن و قطبهای آهنربا حذف شوند. برای این منظور باید سطوح قوه تغذیه میشود میتواند باری به جرم 80 تا 100Kg را نگه دارد.
کاربرد آهنرباهای الکتریکی با نیروی بالا برندگی زیاد :
از آهنرباهای با نیروی بالابرهای بزرگ در مهندسی برای مقاصد گوناگونی استفاده میشود. مثلا ، جرثقیلهایی که با آهنربای الکتریکی کار میکنند، در کارخانههای استخراج فلز و فلزکاری برای حمل تکههای آهن یا ادوات که باید روی آن آشکار شود جذب آهنربای الکتریکی نیرومندی میشود. کافی است که جریان را وصل کنیم تا جسم در هر وضعی بر میز کار ثابت شود، یا جریان را قطع کنیم تا جسم رها شود.
برای جدا کردن مواد مغناطیسی از اجسام غیر مغناطیسی ، نظیر جداسازی سنگآهن از کلوخ «جداسازی مغناطیسی) ، جدا کنندههای مغناطیسی به کار میروند، که در آنها مادهای که باید تصفیه شود از میدان مغناطیسی نیرومند آهنربای الکتریکی میگذرند. این میدان تمام ذرات مغناطیسی را از ماده جدا میکند.
آهنربای الکتریکی پیشرفته :
اخیرا آهنرباهای الکتریکی پرقدرت با سطوح عظیم قطبها کاربردهای مهمی در ساختمان شتابدهندهها یافتهاند، یعنی وسایلی که در آنها ذرات باردار الکتریکی الکترونها و پروتونها) تا سرعتهای بسیار بالایی که به انرژی 108 تا 109 الکترون ولت مربوطند، شتاب داده می شوند. باریکه هایی از چنین ذرات که با سرعت بسیار زیادی حرکت میکنند ابزار عمده ای برای بررسی ساختار اتمیاند. آهنرباهایی که در این وسایل به کار میروند حجمهای عظیمی دارند.
آهنرباهای الکتریکی با قطب های مخروط ناقص :
وقتی که لازم باشد میدان مغناطیسی بسیار نیرومندی را فقط در ناحیه کوچکی بدست میآوریم، آهنرباهای الکتریکی با قطبهایی به شکل مخروط ناقص به کار میروند. آن گاه در فضای کوچک بین آنها میدانی با القای مغناطیسی با 5T را میتوان به آسانی به دست آورد. چنین آهنرباهای الکتریکیای عمدتا در آزمایشگاههای فیزیک برای آزمایشهایی با میدان مغناطیسی نیرومند به کار می روند.
کاربردهای پزشکی آهنرباهای الکتریکی :
انواع دیگر آهنربای الکتریکی نیز برای مقاصد خاصی طراحی شده اند. مثلا ، پزشکها برای خارج کردن برادههای آهن که تصادفی وارد چشم شده باشند از آهنربای الکتریکی استفاده میکنند. برای خارج ساختن سوزن و سایر اشیا تیز فرو رفته در پا و سایر اعضای بدن از آهنرباها استفاده میشود.

مغناطیس
علم مغناطیس از این مشاهده که برخی سنگها (ماگنتیت) تکههای آهن را جذب می کردند سرچشمه گرفت. واژه مغناطیس از ماگنزیا یا واقع در آسیای صغیر ، یعنی محلی که این سنگها در آن پیدا شد، گرفته شده است. زمین به عنوان آهنربای دائمی بزرگ است که اثر جهت دهنده آن بر روی عقربه قطبهای آهنربا ، از زمانهای قدیم شناخته شده است. در سال 1820 اورستد کشف کرد که جریان الکتریکی در سیم نیز میتواند اثرهای مغناطیسی تولید کند، یعنی میتواند سمت گیری عقربه قطب نما را تغییر دهد.
در سال 1878 رولاند (H.A.Rowland) در دانشگاه جان هاپکینز متوجه شد که یک جسم باردار در حال حرکت (که آزمایش او ، یک قرص باردار در حال دوران سریع) نیز منشاأ اثرهای مغناطیسی است. در واقع معلوم نیست که بار متحرک هم ارز جریان الکتریکی در سیم باشد. جهت مطالعه زندگینامه علمی رولاند فیزیکدان برجسته آمریکایی به کتاب زیر مراجعه شود:
Phusics by John D.Miller,Physics
Today , July 1976Rowland،s البته دو علم الکتریسیته و مغناطیس تا سال 1820 به موازات هم تکامل می یافت اما کشف بنیادی اورستد و سایر دانشمندان سبب شد که الکترومغناطیس به عنوان یک علم واحد مطرح شود. برای تشدید اثر مغناطیسی جریان الکتریکی در سیم میتوان را به شکل پیچهای با دورهای زیاد در آورد و در آن یک هسته آهنی قرار داد. این کار را میتوان با یک آهنربای الکتریکی بزرگ ، از نوعی که معمولا در پژوهشگاههای برای کارهای پژوهشی مربوط به مغناطیس بکار میرود، انجام داد.
تولد میدان مغناطیسی
دومین میدانی که در مبحث الکترومغناطیس ظاهر می شود، میدان مغناطیسی است. این میدانها و به عبارت دقیقتر آثار این میدانها از زمانهای بسیار قدیم ، یعنی از همان وقتی که آثار مغناطیسهای طبیعی سنگ آهنربا (Fe3O4 یا اکسید آهن III) برای اولین بار مشاهده شد، شناخته شدهاند. خواص شمال و جنوب یابی این ماده تاثیر مهمی بر دریانوردی و اکتشاف گذاشت با وجود این، جز در این مورد مغناطیس پدیده ای بود که کم مورد استفاده قرار می گرفت و کمتر نیز شناخته شده بود، تا اینکه در اوایل قرن نوزدهم اورستد دریافت که جریان الکتریکی میدان مغناطیسی تولید میکند.
این کار تواأم با کارهای بعدی گاؤس ، هنری . فاراده و دیگران نشان دادند که این شراکت واقعی بین میدانهای الکتریکی و مغناطیسی وجود دارد و این دو توأم تحت عنوان میدان الکترومغناطیسی حضور دارند. به عبارتی این میدانها به طرز جدایی ناپذیری در هم آمیخته شدهاند.

حوزه عمل و گسترش میدان مغناطیسی
تلاش مردان عمل به توسعه ماشینهای الکتریکی ، وسایل مخابراتی و رایانهها منجر شد. این وسایل که پدیده مغناطیسی در آنها دخیل است نقش بسیار مهمی در زندگی روزمره ایفا میکنند. با گسترش و سریع علوم از اعتبار این علوم اولیه کاسته نمیشود و همیشه سازگاری خود را با کشفیات جدید حفظ میکند.
مغناطیسهای طبیعی و مصنوعی
• بعضی از سنگهای آهن یاد شده در طبیعت خاصیت جذب اشیای آهنی کوچک ، مانند برادهها یا میخهای مجاور خود را دارند. اگر تکهای از چنین سنگی را از ریسمانی بیاویزیم ، خودش را طوری قرار میدهد که راستایش از شمال به جنوب باشد، تکههای چنین سنگهایی به آهنربا یا مغناطیس معروف است.
• یک تکه آهن یا فولاد با قرار گرفتن رد مجاورت آهنربا ، آهنربا یا مغناطیده میشود، یعنی توانایی جذب اشیای آهنی را کسب میکند. خواص مغناطیسی این تکه آهن یا فولاد هر چه به آهنربا نزدیکتر باشد، قویتر است. وقتی که تکهای از آهن و آهنربا با یکدیگر تماس پیدا کنند ، مغناطش یا آهنربا شدگی به مقدار ماکزیمم (میخ آهنی که به آهنربا نزدیک شود خاصیت آهنربایی پیدا میکند و برادههای آهنربا را جذب میکند) میباشد.
• هنگامی که آهنربا دور شود، تکه آهن یا فولاد که توسط آهنربا شدهاند بخش زیادی از خواص مغناطیسی بدست آورده را از دست میدهند، ولی باز هم تا حدی آهنربا میمانند. از اینرو به آهنربای مصنوعی تبدیل میشوند و همان خواص آهنربای طبیعی را دارد. این پدیده را میتوان با آزمایش سادهای به اثبات رسانید. خاصیت آهنربایی که به هنگام تماس تکه آهن با آهنربا پیدا میشود بر خلاف مغناطش بازمانده که با دور شدن آهن ربا باقی میماند، مغناطش موقت نامیده میشود. آزمایشهایی از این نوع نشان میدهد که مغناطش بازمانده خیلی ضعیفتر از مغناطش موقت است، مثلا در آهن نرم فقط کسر کوچکی از آن است.
• هم مغناطش موقت و هم مغناطش بازمانده برای درجات مختلف آهن و فولاد متفاوت است. مغناطش موقت آهن نرم و آهن تابکاری شده از آهن نرم و فولاد تابکاری نشده به مقدار زیادی قویتر است. بر عکس مانده مغناطش فولاد ، به ویژه درجاتی از آن که شامل مثلا آمیزه کبالت است، خیلی قویتر از مغناطش باز مانده در آهن نرم است. در نتیجه ، اگر دو میله یکسان ، یکی ساخته شده از آهن نرم و دیگری از فولاد را اختیار کنیم و آنها را در مجاورت آهنربای یکسانی قرار دهیم ، میله آهن نرم قویتر از فولاد آهنربا میشود.
ولی اگر آهنربا را دور کنیم، میله آهن نرم تقریبا بطور کلی مغناطیده میشود، در حالیکه میله فولاد مقدار قابل توجهی از خاصیت آهنربایی اولیه خود را حفظ می کند. در نتیجه ، آهنربای دائمی از میله فولادی از میله آهنی خیلی قویتر است. به این دلیل آهنرباهای دائمی را از درجات خاصی از فولاد درست میکنند نه از آهن.
• آهنرباهای مصنوعی که بطور ساده با قرار دادن تکهای فولاد در نزدیکی یک آهنربا یا با تماس با آن بدست آمده نسبتا ضعیف هستند. آهنرباهای قویتر را با مالیدن تیغه فولادی با آهنربا در یک جهت بدست میآورند. البته در این حالت نیز آهنرباهایی که بدست میآید که از آهنربایی که مغناطش به توسط آن انجام شده است، ضعیفتر است. هر نوع ضربه یا تکانی در طول مغناطش عمل را آسانتر میکند. برعکس تماس دادن آهنربای دائمی با تغییر ناگهانی و زیاد دمای آن ممکن است باعث وامغناطش آن شود.
• وامغناطش بازمانده نه تنها به ماده بلکه به شکل جسمی که آهنربا میشود نیز بستگی دارد. میلههای نسبتا کوتاه و کلفت از آهن نرم بعد از دور شدن آهنربا تقریبا به کلی خاصیت آهنربایی را از دست میدهند. با وجود این ، اگر همین آهن را برای ساختن سیمی به طول 300 تا 500 برابر قطر آن بکار بریم، این سیم (ناپیچیده) خاصیت مغناطیسی خود را به مقدار زیادی حفظ خواهد کرد

| | نسخه قابل چاپ | تعداد بازديد : 10760 |
نور خورشید
نور خورشید شامل امواج رادیویی، اشعه فروسرخ، نور مرئی، اشعه فرا بنفش، اشعه ایکس و اشعه گاما. مایکروویو ها،( که موج های بسیار قوی رادیوئی هستند، گاهی در یک رده دیگر به طور مجزا قرار می گیرند.) هستند. پرتوهای خورشید شامل همه پرتوهای طیف الکترومغناطیس می باشند.
منجمان برای مشاهده یک ستاره و تجزیه تحلیل آن فقط می توانند از امواج مغتاطیسی تولید شده از آن را مورد برسی قرار دهند.
به عنوان مثال خورشید با چشم در طول موج مرئی به این صورت دیده می شود




دیدن در طول موج مرئی
دیدن در طول موج رادیویی
دیدن در طول موج ایکس
موج الکترومغناطیسی بعد از تولید شدن از خورشید با سرعت نور در همه جهات پخش می شود و در یکی از این جهات به سمت زمین می آید.پس از برخورد این موج به جو زمین مقداری منعکس و مقداری وارد جو می شود.درجو زمین بعضی از طول موج ها جذب جو می شود و بعضی از به زمین می رسد. در شکل زیر می توانید مقدار نفوذ این امواج را ببینید.

بسته به طول موج امواج، این امواج وارد زمین می شوند.هرچه طول موج بیشتر باشد،امواج بیشتر وارد جو زمین می شود و هرچه طول موج ها کمتر یاشد بیشتر در جو زمین جذب می شوند و کمتر به زمین می رسند
از این لحاظ امواج رادیویی از همه امواج بیشتر وارد زمین می شوند و امواج گاما و ایکس در جو زمین گیر می کنند و وارد سطح زمین نمی شوند.موج بنفش به علت انرژی زیادی که دارد(طول موج کم) بیشتر منعکس می شود به همین علت آسمان به رنگ بنفش می شود ولی به علت اینکه چشم انسان نور آبی را بهتر می بیند آسمان به صورت آبی در می آید
در زیر موج الکترومغناطیسی که با چشم قابل دیدن هست را می بینید.خارج از طول موج مرئی با چشم قابل دیدن نمی باشد و این به علت اثر نداشتن بر روی سلول های شبکیه چشم می باشد
انرژی زیاد . طول موج کم
<<طول موج مرئی>>
انرژی کم .طول موج زیاد

به علت وارد نشدن تمامی امواج الکترومغناطیس به سطح زمین،دیدن ستارگان و تحقیق در مورد آنها مشکل می شود به همین دلیل برای دیدن این ستاره ها در طول موج های پایین باید از جو زمین خارج شد .چون امواج با طول موج پایین از جو زمین عبور نمی کنند و بیشتر منعکس می شوند. ولی برای مطالعه ستاره ها در طول موج بالا مثل رادیویی نیازی به این کار نمی باشد و بر روی زمین هم می توان این مشاهدات را انجام داد.
برای پی بردن مواد تشکیل دهنده ستاره آن را در طول موج مرئی مورد برسی قرار می دهند به طورمثال بعد از گرفتن طول موج های مرئی ستاره ،چنین چیزی مشاهده می شود (عکس پایین). در طیف سنجی اثبات شده که در اثر تحریک اتمی اتمها بنا به ترازهای انرژی مشخصی که دارند تنها میتوانند در ناحیه مشخصی از این باند طول موجی تابش نمایند.بنابر این هر عنصر موجود در ترکیب خطوط مربوط به خود را در تابش طیفی خواهد داشت
به وسیله این شکل می توان مواد تشکیل دهنده این ستاره را از نمودار زیر مشاهده نمود

بیشتر بخوانید:
سفرانسان به مریخ بابلیطی یکطرفه

قدم نهادن انسان بر روی سیاره مریخ مطابق با فناوری و دانش قرن ۲۱ میلادی حقیقتا دست یافتنی است، البته اگر سفری یک طرفه را در نظر بگیریم!
در سال گذشته لارنس کراوس، دانشمند فیزیکدان، در نیویورک تایمز مقاله ای با مضمون: “بلیط یک طرفه به مریخ” نوشت و این سفر وسوسه انگیز را با موارد علمی پیش بینی و بررسی کرد.
امروز برای سفر انسان به مریخ مشکلی بابت امکانات پرواز فرا زمینی یا سیستم حمل و نقل و سوخت مورد نیاز در این سطح نیست بلکه مشکل پرتو های الکترومغناطیسی در تمام طیف و حامل انرژی های مخرب است که از سوی خورشید به تمام جهات منظومه شمسی منتشر می شوند. این پرتو ها آن قدر انرژی دارند که هر موجود زنده ای را به بخارش تبدیل کنند! علمی تر بخوام بگم طیف گسترده و پر انرژی امواج الکترومغناطیسی که خورشید ساطع می کند، دی ان ای هر موجود زنده ای را تجزیه می کند. و هر فضانوردی که بخواد از سیاره مقصد یعنی مریخ به زمین برگردد با شروع سفرش خواهد مرد. استفاده از سپر های محافظ هم با فناوری امروزی بسیار پر جرم خواهند بود به طوری که برای یک سفر عادی برگشت سپر محافظی به وزن ۴۰۰ تن نیاز خواهد بود. اما برای سفر رفت تاثیر این پرتو های خورشیدی کمتر و تغییر می کند و با سپر محافظ معمول تری سفر رفتن هر چند گران قیمت ولی امکان پذیر می شود.
به همین خاطر سفر رفت واقع گرایانه است ولی برگشتی در کار نخواهد بود. در مقاله سفر یکطرفه به مریخ، کراوس توصیه می کند که هر کاری که انسان اولیه در مریخ قرار است انجام بدهد را می توان از بازوی توانمند روبات ها انتظار داشت و انسان های داوطلب هم می توانند جمع شوند تا ماه های آخر عمرشان را در سیاره سرخ و ناشناخته بگذرانند و آزمایش ها و تجربیات اولیه را به اجرا بگذارند و قدمی در راه پیشرفت در این زمینه باشند.
به هر حال برای سفری بازگشت پذیر با بلیطی دو طرفه به مریخ نیاز به پیشرفت فوق العاده در فناوری های موشکی و حمل و نقل نیست بلکه نیاز به اکتشافات و پیشرفت هایی در فناوری های پزشکی و مخابراتی است تا به نحوی ساده تر با پرتوهای زیان بار خورشیدی مقابله کرد.
با پرتو های خطر ناک خورشیدی بیشتر آشنا بشیم:
طیف امواج الکترو مغناطیسی خورشید و فضای خارج از کره زمین شامل همه چی میشه: امواج صوتی (موج الکترومغناطیسی نیست)، رادیویی، مایکروویو، فروسرخ، نور مرئی، فرابنفش، پرتو ایکس، گاما و پرتو های کیهانی
امواج قوی تر از نور مرئی (انرژی بالاتر در امواج الکترومغناطیسی با طول موج کمتر و فرکانس بالاتر همراه است) برای انسان و هر موجود زنده دیگری کشنده است و کره زمین با سیستم های محافظتی مختلف جلوی ورود غالب این امواج به درون جو خودش را می گیرد، لایه اوزون، یونسفر، وجود جوی مناسب و سیستم مغناطیسی زمین در قطبین عاملان اصلی جلوگیری از تخریب حیات آن هستند. اما در خارج از محدوده سیاره ما و حتی در جو سیاره مریخ دیگر این سپر های محافظتی سیاره زنده زمین وجود ندارد و این امواج به راحتی عبور می کنند و بر سطح مریخ تاثیر می گذارند.
به همین خاطر از مهم ترین عوامل منفی در سفر های فضایی برای انسان این پرتو های نابودگر می باشد که امید است با پیشرفت ها لازم راهی برای مقابله با آن پیدا کرد که البته در آینده دور نخواهد بود و به زودی شاهد خبر هایی در این مورد خواهیم بود.
| | نسخه قابل چاپ | تعداد بازديد : 73 |
پیلهای الکتروشیمیایی ابزاری برای تبدیل انرژی الکتریکی و شیمیایی به یکدیگر بوسیله واکنشهای الکتروشیمیایی هستند، بدین دلیل به اسم پیلهای الکتروشیمیایی معروفند.
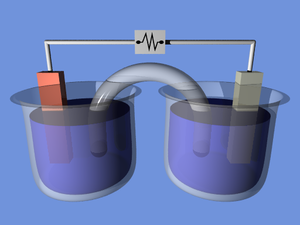
پیلهای الکتروشیمیایی ابزاری برای تبدیل انرژی الکتریکی و شیمیایی به یکدیگر بوسیله واکنشهای الکتروشیمیایی هستند، بدین دلیل به اسم پیلهای الکتروشیمیایی معروفند.
مقدمههنگامی که چراغ قوه را روشن کنید یا برای روشن شدن خودرو استارت میزنید از انرژی الکترکی استفاده میکنید. این انرژی توسط دستهای از واکنشهای شیمیایی فراهم میشود که در باتریها روی میدهد. مطالعه شیمی باتریها و مباحثی برقکافت ، آبکاری ، فلز گری و از همه مهمتر خوردگی که در چالش برانگیزترین مسأله در جوامع صنعتی امروز به شمار میآید همگی در نتیجه واکنشهای الکتروشیمیای مطرح میشوند.
تاریخچهالکساندر ولتا (1827 - 1745) فیزیکدان ایتالیایی و مخترع اولین باتری است که اکنون پیل ولتا نامیده میشود. این پیل شامل صفحات متناوبی از مس و روی است که توسط صفحات مقوایی نازک که در محلول نمکی غوطهورند از هم جدا شدهاند، بخاطر کمک او به علم الکتریسیته ، واحد اختلاف پتانسیل الکتریکی (ولت) به نام اوست.
نقش و تأثیر در زندگیباتریهای خشک در زندگی روزمره برای مصارف گوناگون بکار میروند، سلولهای انبارهای که شامل باتری خودرو باشند برای راه اندازی اتومبیلها بکار میروند، از باتریهای نیکل - کادمیم در ابزاری مانند تلفن بی سیم ، رایانههای قابل حمل (لپ تاپ) ، تلفن همراه و ماشینهای اصلاح استفاده میشود و سلولهای سوختی برای تأمین برق و آب آشامدنی فضاپیما استفاده میشود و برای تأمین برق بیمارستانها و به تازگی تأمین نیروی محرکه وسایل نقلیه سنگین و سبک هم استفاده میشود. خوردگی سالانه خسارات زیادی در صنعت به بار میآورد.
ساختار یا ساختمانیک پیل الکتروشیمیایی از دو الکترود جریان به نام الکترود کاتد و آند تشکیل یافته است، به هر یک از این الکترودها که در محلول الکترولیت قرار گرفتهاند و محلولهای الکترولیتی در صورت متفاوت بودن از نظر ترکیب شیمیایی توسط یک پیل نمی که لولههای شیشهای نعلی شکل پر شده از محلول غلیظ یک الکترولیت قدیمی باشند و یا یک دیواره متخلخل (نظیر شیشه گداخته و یا چینی و سرامیک بدون لعاب) باهم ارتباط دارند. پیهای الکتروشیمیایی بطور قرار دادی به دو نوع پیل گالوانیک (ولتایی) و الکترولیزی تقسیم میشوند.
طرز کار و مکانیزم کارپیلهای الکتروشیمیایی با واکنشهای اکسایش - کاهش: واکنشهای اکسایش- کاهش عبارتند از انتقال الکترون از یک واکنشگر به واکنشگر دیگری. واکنش اکسایش - کاهش از دو نیم واکنش تشکیل یافته است، نیم واکنشی که در آن واکنشگر الکترون از دست میدهد نیم واکنش اکسید است و در آند رخ میدهد و واکنشگر را کاهنده یا احیا کننده پیلهای الکتروشیمیایی مینامند. نیم واکنشی که در آن واکنشگر الکترون میگردد، نیم واکنش احیا یا کاهش میباشد و در کاتد رخ میدهد و واکنشگر را اکسید کننده یا اکسنده مینامند و پتانسیل واکنش را میتوان با استفاده از معادله ارنست محاسبه کرد.
کاربردهااز پیلهای الکتروشیمیایی میتوان در موارد زیر استفاده نمود:
تعیین PH محیط واکنش و ثابت تعادل واکنش در صنعت نانو برای رسوب گیری مواد بر روی الکترودها در ساخت و کاربرد حسگرها مورد استفاده در تشخیص و اندازه گیری گونههای زیستی یعنی زیست حسگرها در صنعت پزشکی برای رسم الکتروکار دیاگرام چشم انداز و آینده بحثمواد قابل سنجش متعددی در هوا ، آب ، خاک و دیگر تشکیل دهندههای محیط زیست وجود دارد و هر روز بر تعداد اینگونه مواد افزوده میشود. ضرورت اندازه گیری آلایندههایی نظیر انواع حشره کشها ، کودهای شیمیایی ، زبالهها و پسابهای صنعتی و خانگی بر کسی پوشیده نیست. با استفاده از پیلها و اندازه گیری پتانسیل آنها به ویژه زیست حسگرها میتوان کلیه امور را در مدت زمان کم و به آسانی انجام داد.
منبع: سایت رشد
| | نسخه قابل چاپ | تعداد بازديد : 66 |
 قدیمیترین دی.ان.ای زمین با عمر ۴۰۰ میلیون سال کشف شد
قدیمیترین دی.ان.ای زمین با عمر ۴۰۰ میلیون سال کشف شد  محققان با دستیابی به ساختار دستنخورده دی.ان.ای متعلق به 419 میلیون سال پیش از اعماق رسوبات نمکی، موفق به کشف قدیمیترین گونه حیات روی زمین شدهاند. آیا داستان پارک ژوراسیک به واقعیت میپیوندد؟
محققان با دستیابی به ساختار دستنخورده دی.ان.ای متعلق به 419 میلیون سال پیش از اعماق رسوبات نمکی، موفق به کشف قدیمیترین گونه حیات روی زمین شدهاند. آیا داستان پارک ژوراسیک به واقعیت میپیوندد؟محبوبه عمیدی: اینکه زمین روزی به یک پارک ژوراسیک بزرگ تبدیل شود، اصلا ایده جالبی نیست، اما واقعیت این است که دانشمندان موفق شدهاند از اعماق رسوبات نمکی میشیگان، قطعات دی.ان.ای دستنخوردهای را کشف کنند که 419 میلیون سال عمر دارند و به حیات بازگشتهاند.
به گزارش دیسکاوری، این قطعات که بدون شک قدیمیترین مواد ژنتیکی روی کره زمین هستند که بشر تاکنون موفق به کشف آنها شده، به باکتری نمکدوستی تعلق دارند که اجدادش میتوانند جزیی از اولین گونههای حیات شکلگرفته روی کره زمین باشند.
پیش از این دانشمندان ماده ژنتیکی مشابهی را از این منطقه استخراج کرده بودند، اما شباهت بسیار دی.ان.ای کشفشده به نمونههای کنونی مانع از این شد که به قدمت چند صدمیلیون ساله آن پی ببرند.
اما اینبار گروهی از محققان دانشگاه دالهوزی در هالیفاکس، کانادا موفق به یافتن شش قطعه دی.ان.ای در این حوضه شدند که هیچ نمونه مشابهی نداشتند.
راسل ویلند از دانشگاه وستچستر میگوید: «ما تمامی توالیهای متعلق به باکتریهای نمکدوست شناختهشده را با این نمونهها مقایسه کردیم. این شش قطعه بینظیر بودند».
بازخوانی شجرهنامه این میکروارگانیسم نشان داد که متعلق به خانوادهای از باکتریهای نمکدوست است که پیش از این هم احتمال وجود آنها در ابتدای حیات روی زمین پیشبینی شده بود.
اولینبار در سال 1930/ 1309 نمونههای زندهای از Halobacterium salinarum متعلق به این خانواده، بر روی پوست یک گاومیش نمکسودشده کشف شد که دانشمندان با توجه به ساختار ژنتیکی این باکتری، آن را یک گونه امروزی فرض کردند. اما تحقیقات این تیم نشان میدهد، H. salinarum در واقع خویشاوندی وراثتی نزدیکی با باکتریهایی دارد که بین 121 و 419 میلیون سال پیش روی کره زمین زندگی میکردهاند.
این تیم با ردگیری محل اولیه کشف پوست گاومیش به نتایج جالب توجهی دست یافت. این پوست از معدنی حوالی ساسکاچوان کشفشده بود، جایی که زمینشناسان معتقدند حدود 300 میلیون سال پیش دریا به خشکی تبدیل شده است.
این باکتری تمام این سالها را میان آب اشباع درگیر در ساختار بلورهای نمک دوام آورده، تا باز هم زمان مناسب برای رشد و تکثیر از راه برسد، یا شاید انسان با جستجو آنرا به حیات برگرداند.
ملانی مورمیل از دانشگاه میسوری در اینباره میگوید: «هر روز با مدارک تازهای مبتنی بر بقا و ادامه حیات این باکتریها مواجه میشویم. آنها به شکل اسرارآمیزی میلیونها سال در اعماق زمین دوام آوردهاند و از تمام یخبندانها و انقراضهای بزرگ جهان جان سالم به در بردهاند، تا امروزه هر کجا که آب شور وجود دارد، زندگی را از سر بگیرند».
ویلند میگوید: «این تنها یک مثال بینقص از تلاش میکروارگانیسمها برای بازگشت به زندگی نیست، بلکه نشان میدهد کره زمین چگونه دارد برای ادامه بقا تلاش میکند».
منبع: همشهری آنلاین
| | نسخه قابل چاپ | تعداد بازديد : 32 |
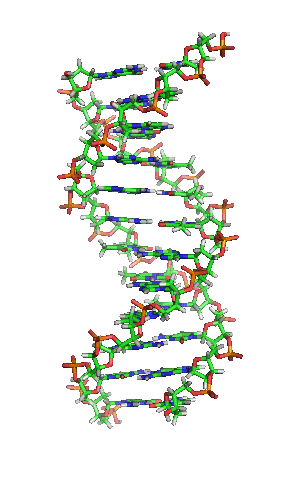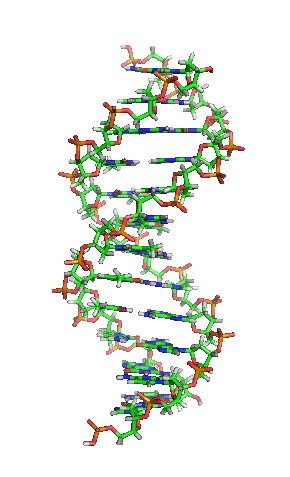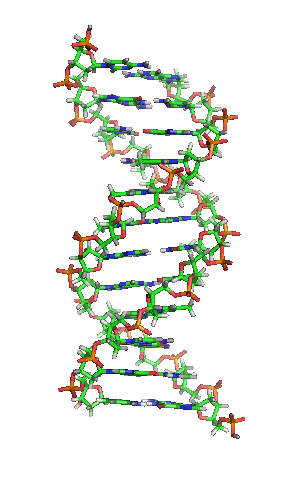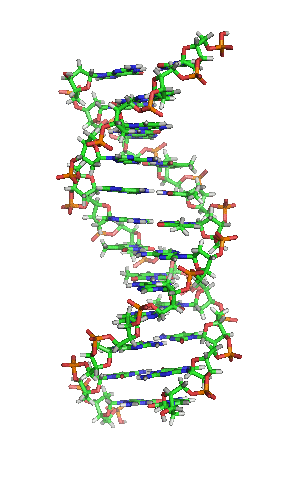
دیانای یکی از ماکرومولکولهای زیستی میباشد که در انتقال دادههای ژنتیکی نقش دارد. این ماکرومولکول، پلیمری از زیرواحدهای نوکلئوتیدی است.
DNAدارای ساختمانی مارپیچی است و برای اولین بار ساختمان آن را دو دانشمند به نام های جیمز واتسون و فرانسیس کریک را در سال ۱۹۵۳ کشف کردند و به همین دلیل جایزه نوبل دریافت کردند. کارکرد اصلی DNA الگو بودن برای ساخته شدن یک اسید نوکلئیک دیگر به نامRNA است.
DNA ماکرومولکولی است که از هر نظر، برای ایفاء مهمترین نقش خود یعنی انتقال اطلاعات بیولوژیک شایسته است. بعبارتی DNA شاهکار خلقت در ایجاد ماکرو مولکولهای زیستی بحساب میآید. همه فواصل و زوایای پیوند، انرژی ها و نوع پیوند عناصر از دقیقترین قوانین فیزیک مولکولی پیروی میکنند. دانشمندان بارها سعی کردهاند با ساخت ماکرومولکولهای دیگری، بتوانند جایگزینی برای DNA بیابند. اما تاکنون تلاشهای آنها با شکست روبرو شده است. از دید بسیاری از محققان،DNA متکاملترین مولکول ایجاد شده توسط طبیعت میباشد. مشخصه مهم ملکول DNA، بهعنوان یک مولکول، هوشمندی آن است. دو رشته DNAکه از نظر توالی بازها، مکمل یکدیگرمی باشند، میتوانند یکدیگر را شناسایی کرده، پیوند هیدروژنی برقرار کنند و این، آن چیزی است که دانشمندان را قادر ساخته است تا از DNA در واکنشهای شیمیایی استفاده کنند.
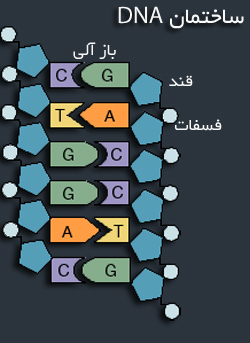
DNAدارای سه بخش ساختمانی است: بازهای نوکلئوتیدی آدنین (A) سیتوزین (C) گوانین (G) و تیمین (T) در پلههای این ماکرومولکول نردبانی قرار دارند. این بازهای نوکلئوتیدی به طور تصادفی در کنار هم قرار ندارند بلکه تیمین به آدنین با پیوند هیدروژنی وصل است و سیتوزین نیز به گوانین با پیوند هیدروژنی اتصال دارد. مولکول های قند دزوکسی ریبوز در دیوارهای این نردبان دیده می شوند و به این مولکول های قند گروههای فسفات متصل هستند. فرق بین قند دزوکسی ریبوز در DNA با قند ریبوز در RNA این است که قند دزوکسی ریبوز یک گروه هیدروکسیل از قند ریبوز کمتر دارد.
آرانای
RNA یا ریبو نوکلئیک اسید یک اسید نوکلئیک در سلول است. RNA را DNA در هسته سلول می سازد. RNA در سه نوع tRNA (مخفف transfer RNA) یا RNA ترابر، mRNA (مخفف messenger RNA) یا RNA پیامبر و rRNA (مخفف ribosomal RNA) یا RNA ریبوزومی است. کار rRNA ساختن پروتئین در ریبوزوم است.
RNA دارای سه بخش ساختمانی است: بازهای نوکلئوتیدی اوراسیل (U) سیتوزین (C) گوانین (G) وآدنین(A) را داراست و برخلاف DNA فاقد تیمین (T)است. مولکول های قند ریبوز و گروههای فسفات از دیگر بخش های RNA است. قند ریبوز در RNA یک گروه هیدروکسیل از قند دزوکسی ریبوز در DNA بیشتر دارد.
فرانسیس کریک
'فرانسیس کریک کاشف ساختار DNA و برنده جایزه نوبل میباشد. کریک در ۸ ژوئن ۱۹۱۶ در انگلستان به دنیا آمد. در رشته فیزیک تحصیلاتش را ادامه داد و پس از جنگ جهانی دوم راه دیگری درپیش گرفت که در سال ۱۹۵۳ همراه جیمز واتسون موفق به کشف ساختار دورشتهای DNA شد ودر سال 1962 موفق به دریافت جایزه نوبل شد . دکترکریک هنگام اعلام این کشف مهم گفت که بشر با کشف تازه بر گوشه ای از اسرار حیات دست یافته است. وی گفت که همه موجودات ذی حیات دارای DNA هستند که دو وظیفه مهم دارد ؛ یکی حمل اطلاعات و دیگری به وجود آوردن المثنای خود. در سن ۸۸ سالگی در بیمارستانی در سان دیگو آمریکا بر اثر سرطان روده بزرگ درگذشت.
نوکلئوتیدنوکلئوتید واحد سازنده اسیدهای نوکلئیک میباشند که ترکیبی متشکل از یک قند ۵-کربنی ( ریبوز یا داکسی ریبوز ) اسید فسفریک (فسفات) و یکی از بازهای آلی پورین (آدنین، گوانین)یا پیریمیرین (سیتوزین، تیمین، اوراسیل) میباشند.اغلب نوکلئوتیدرا نوکلئوزید فسفات می گویند.نوکلئوتیدها به دلیل اسید فسفریک ترکیب اسیدی هستند.
به مجموعه قند و باز آلی نوکلئوزید گفته میشود. گروه فسفات میتواند قند متصل شود. به مجموع نوکلئوزید و گروه فسفات متصل به و یا5 به کربن3 آن نوکلئوتید میگویند. با توجه به اینکه یون فسفات میتواند هم به کربن متصل شود. و هم به کربن5 3
پس دو نوکلئوتید از طریق یک پیوند فسفودی استر بهم متصل میشوند. به این صورت که گروه هیدروکسیل یک نوکلئوتید با گروه فسفات نوکلئوتید دیگر واکنش داده و پیوند فسفودی استر را بوجود میآورد. از آنجایی که پیوند دو قند مجاور را بهم متصل میکند، این پیوند و5 فسفودی استر ، کربنهای3 فسفودی استر نیز مینامند. یک زنجیره در اثر اتصال پشت سر -3 را پیوند5 -دزوکسی ریبونوکلئوتید بوسیله پیوندهای دزوکسی ریبونوکلئوتید هم تعدادی2 تشکیل میشود
تمامی نوکلئوتیدها در یک زنجیره پلی نوکلئوتیدی دارای جهت یکسان میباشند. به این صورت که نوکلئوتید انتهایی در یک سمت زنجیره دارای یک آزاد آزاد و نوکلئوتید انتهایی در سمت دیگر زنجیره دارای یک گروه3 گروه5 میباشد. بنابراین زنجیره پلی نوکلئوتیدی دارای جهت بوده و این جهت را به --- صورت5> نشان میدهند. بنابراین اگر در نوکلئوتید ابتدایی کربن5 3 در زیر آن باشد، در تمامی نوکلئوتیدهای بعدی در بالای حلقه پنتوز و کربن3 زنجیره کربن 5 در بالای حلقه پنتوز جای خواهد داشت.
ژنتیک مولکولی
ژنتیک و زیست شناسی مولکولی دو موضوع کاملا مرتبط بهم هستند و اگر چه تفاوتهایی بین آنها موجود است، ولی بهتر است که آنها را در یک قالب مطرح کرد. به این دلیل اصطلاح ژنتیک مولکولی امروزه اغلب برای تشریح شاخهای از زیست شناسی بکار میرود که مربوط به مطالعه همه جنبههای یک ژن است
ماهیت مولکولی ماده ژنتیکی چیست؟ چطور اطلاعات ژنتیکی از یک نسل به نسل بعد با صحت بالا انتقال مییابد؟ تغییرات نادر در ماده ژنتیکی که ماده خام تکامل میباشد، چگونه ایجاد میشوند؟ چطور اطلاعات ژنتیکی نهایتا به شکل توالیهای اسید آمینهای مولکولهای پروتئینی متنوع موجود در یک سلول زنده ، بیان میشود؟ و ... . واحد پایه اطلاعات در سیستمهای زنده ، ژن میباشد.
از نظر بیوشیمیایی یک ژن به صورت قطعهای از DNA تعریف میشود که اطلاعات مورد نیاز برای ایجاد یک محصول دارای فعالیت بیولوژیک راکد میکند. محصول نهایی معمولا یک پروتئین است. ممکن است محصول ژنی وظیفهای یکی از انواع RNA باشد. ذخیره ، حفظ و متابولیزم این واحدهای اطلاعاتی موضوعات بحث را در ژنتیک مولکولی تشکیل میدهند. پیشرفتهای اخیر در ژنتیک مولکولی ، منجر به مطرح شدن سه فرآیند اصلی در استفاده از اطلاعات ژنتیکی شده است.
اولین فرآیند ، همانند سازی DNA یا نسخه برداری از DNA مادری و تولید مولکولهای DNA با توالیهای نوکلئوتیدی یکسان میباشد.
دومین فرآیند سنتز RNA از روی DNA است، که طی قسمتهایی از پیام ژنتیکی کد شده در DNA دقیقا به صورت RNA ، نسخه برداری میشود.
سومین فرآیند ، ترجمه میباشد که به موجب آن پیام ژنتیکی کد شده در RNA پیک بر روی ریبوزومها به پلیپپتیدی با توالی مشخص از اسیدهای آمینه ترجمه میشود.
وقایع مهم در ژنتیک مولکولی تا سال ۱۹۴۴
شروع ژنتیک توسط گرگور مندل و با مقالهای بود که وی در سال ۱۸۶۶ در مجموعه مقالات انجمن علوم طبیعی در مورد نخود فرنگی ، به چاپ رساند.
تا سال ۱۹۰۰ طول کشید تا سایر زیست شناسان مانند هوگو ، کورنس و شرماک اهمیت کار مندل را درک کنند و این علم پس از رکورد طولانی توالی دوباره یافت.
در سال ۱۹۰۳ ، ساتن پیشنهاد کرد که ژنها روی کروموزومها قرار دارند.
در سال ۱۹۰۹ ، یوهانس پیشنهاد کرد که عوامل مندلی ژن نامیده شدند.
در سال ۱۹۱۰ ، مورگان آزمایشهای زیادی بر روی مگس سرکه انجام داد.
در سال ۱۹۲۷ ، مولر کشف کرد که اشعه ایکس ایجاد موتاسیون (جهش) در مگس سرکه مینماید.
در سال ۱۹۴۱ ، بیدل و تاتوم پیشنهاد کردند که هر ژن فعالیت یک آنزیم را کنترل میکند.
در سال ۱۹۴۴ ، کتاب زندگی چیست توسط یک فیزیکدان به نام شرودینگر انتشار یافت.
کشف ساختمان DNA
شناخت امروزی ما در مورد مسیرهای اطلاعاتی از همگرایی یافتههای ژنتیکی ، فیزیکی و شیمیایی در بیوشیمی امروزی حاصل شده است. لین شناخت در کشف ساختمان دو رشته مارپیچی DNA ، توسط جیمز واتسون و فرانسیس کریک در سال ۱۹۵۳ خلاصه گردید. فرضیه ژنتیکی ، مفهوم کد نمودن توسط ژنها را مشخص نمود. با استفاده از روشهای فیزیکی ، تعیین ساختمان مولکولی DNA بوسیله آزمایش انکسار اشعه ایکس ممکن گردید. شیمی نیز ترکیب DNA را آشکار نمود. ساختمان مارپیچی دو رشتهای DNA ، چگونگی نسخه برداری آن را نشان داد، نحوه تولید RNA و سنتز پروتئین از روی آن را شفاف کرد.
ژنها و کروموزومها
ژنها قطعاتی از یک کروموزوم هستند که اطلاعات مورد نیاز برای یک مولکول DNA یا یک پلی پپتید را دارند. علاوه بر ژنها ، انواع مختلفی از توالیهای مختلف تنظیمی در روی کروموزومها وجود دارد که در همانند سازی ، رونویسی و ... شرکت دارند. کروموزومهای یوکاریوتی دارای دو توالی مهم تکراری DNA میباشند که عمل اختصاصی را انجام میدهند؛ سانترومرها که نقاط اتصالی برای دوک تقسیم هستند و تلومرها که در دو انتهای کروموزوم وجود دارند. کروماتین در یوکاریوتها به صورت واحدهای نوکلئوزومی قرار دارد.
متابولیزم DNA
سلامت DNA بیشترین اهمیت را برای سلول دارد که آن را میتوان از پیچیدگی و کثرت سیستمهای آنزیمی شرکت کننده در همانند سازی ، ترمیم و نوترکیبی DNA ، دریافت. همانند سازی DNA با صحت بسیار بالا و در یک دوره زمانی مشخص در طی چرخه سلولی به انجام می رسد. همانند سازی نیمه حفاظتی است، بطوری که هر رشته آن به عنوان قالبی برای تولید رشته جدید DNA مورد استفاده قرار میگیرد. سلولها دارای سیستمهای متعددی برای ترمیم DNA هستند. توالیهای DNA در طی واکنشهای نوترکیبی ، در فرآیندهایی که شدیدا هماهنگ با همانند سازی یا ترمیم DNA هستند، نو آرایی میشوند.
متابولیزم RNA
رونویسی توسط آنزیم RNA پلیمراز وابسته به DNA کاتالیز میشود. رونویسی در چندین فاز ، شامل اتصال RNA پلیمراز به یک جایگاه DNA به نام پروموتور ، شروع سنتز رونویسی ، طویل سازی و خاتمه ، روی میدهد. سه نوع RNA ساخته میشود؛ RNA پیک که برای ساختن پلی پپتیدها مورد استفاده قرار میگیرد. RNA ناقل که در انتقال اسیدهای آمینه بر روی ریبوزومها برای پروتئین سازی ، شرکت دارند و RNA ریبوزومی که در ساختار ریبوزوم شرکت دارند. این RNA ها به صورت پیش ساز ساخته میشوند که طی فرآیندهای آنزیمی بالغ میشوند.
متابولیزم پروتئین
پروتئینها در یک کمپلکس RNA پروتئینی به نام ریبوزوم ، با یک توالی اسید آمینههای خاص در طی ترجمه اطلاعات کد شده در RNA پیک ، سنتز میگردند. اسیدهای آمینهای که توسط کدونهای RNA پیک مشخص میگردند، از کلمات سه حرفی نوکلئوتیدی تشکیل شدهاند. برای ترجمه نیاز به مولکولهای RNA ناقل میباشد که با شناسایی کدونها ، اسیدهای آمینه را در موقعیتهای متوالی مناسب خود در داخل زنجیر پلی پپتیدی قرار میدهند. بعد از سنتز بسیاری از پروتئینها به موقعیتهای خاص خود در داخل سلول هدایت میشوند.
تنظیم بیان ژن
بیان ژنها توسط فرآیندهایی تنظیم میشود که بر روی سرعت تولید و تخریب محصولات ژنی اثر میگذارند. بیشتر این تنظیم در سطح شروع رونویسی و بواسطه پروتئینهای تنظیمی رخ میدهد که رونویسی را از پروموتورهای اختصاصی مهار یا تحریک میکنند. اثر مهارکننده ها را تنظیم منفی و فعال شدن را تنظیم مثبت گویند. پروتئینهای تنظیمی ، پروتئینهای اتصالی DNA هستند که توالیهای اختصاصی از DNA را شناسایی میکنند. هورمونها بر روی تنظیم بیان ژن تأثیر دارند. موجودات یوکاریوت و پروکاریوت دارای مکانیزمهای متفاوتی برای تنظیم بیان ژنهای خود دارند.
فناوری DNA نوترکیبی
با استفاده از فناوری DNA نو ترکیبی مطالعه ساختمان و عملکرد ژن بسیار آسان شده است. جداسازی یک ژن از یک کروموزوم بزرگ نیاز دارد به، روشهایی برای برش و دوختن قطعات DNA ، وجود ناقلین کوچک که قادر به تکثیر خود بوده و ژنها در داخل آنها قرار داده میشوند، روشهایی برای ارائه ناقل حاوی DNA خارجی به سلولی که در آن بتواند تکثیر یافته و کلنیهایی را ایجاد کند و روشهایی برای شناسایی سلولهای حاوی DNA مورد نظر. پیشرفتهای حاصل در این فناوری ، در حال متحول نمودن بسیاری از دیدگاههای پزشکی ، کشاورزی و سایر صنایع میباشد
| | نسخه قابل چاپ | تعداد بازديد : 163 |

الکتریسیته در همه جای زندگی ما دیده می شود، الکتریسیته خانه ها را روشن می کند ، غذای ما را می پزد ، نیروی لازم برای کامپیوتر ، تلویزیون و دیگر وسایل الکترونیکی را تامین می کند. الکتریسیته ی باتری ها ، چراغ قوه را در تاریکی روشن می کند و ماشین ما را به حرکت در می آورد.
می توانید کاری کنید تا بفهمید الکتریسیته تا چه اندازه مهم است. به سمت مدرسه یا خانه خود بروید و وسایل و ماشین های مختلفی که از الکتریسیته استفاده می کنند را بنویسید . از تعداد زیاد چیزهایی که ما هر روزه استفاده می کنیم و به الکتریسیته وابسته است متعجب خواهید شد.
اما الکتریسیته چیست ؟ از کجا آمده است؟ چطور کار می کند؟
قبل از این که همه این ها را بفیمهیم ، باید کمی درباره اتم ها و ساختار آن ها بدانیم.
همه مواد از اتم ها و اتم ها از ذرات کوچک تری ساخته شده اند. سه ذره اصلی که اتم ها را می سازد پروتون ، الکترون و نوترون است.
الکترون ها به دور مرکز یا هسته اتم می چرخند همان طور که ماه به دور زمین می گردد. هسته از نوترون و پروتون تشکیل شده است.
الکترون ها شامل یک بار منفی و پروتون ها یک بار مثبت هستند ، نوترون ها خنثی هستند آن ها نه بار مثبت دارند نه بار منفی.
انواع مختلفی از اتم ها وجود دارد، هر یک از این انواع، یک عنصر است، اتم تنها قسمت سازنده عنصر است. 118 نوع عنصر شناخته شده وجود دارد، بعضی عناصر مانند اکسیژنی که ما با آن نفس می کشیم برای حیات ضروری است.
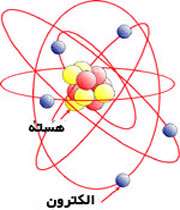
در هر اتم تعداد مشخصی الکترون ،پروتون و نوترون وجود دارد، اما معمولاً جدا از این که یک اتم چند ذره دارد، تعداد الکترون ها باید با تعداد پروتون ها برابر باشد. اگر تعداد الکترون ها و پروتون ها یکی باشد، اتم در تعادل و بسیار پایدارد است.
بنابراین، اگر یک اتم 6 پروتون داشته باشد، باید 6 الکترون نیز داشته باشد، عنصری با 6 پروتون و 6 الکترون، کربن نامیده می شود، کربن در خورشید، ستاره ها، ستاره های دنباله دار، اتمسفر بیشتر سیاره ها و مواد غذایی که می خوریم به مقدار زیادی وجود دارد، ذغال سنگ و الماس نیز از کربن ساخته شده است.
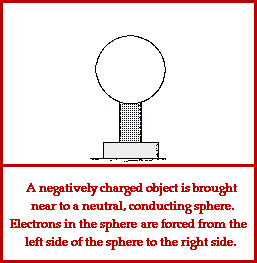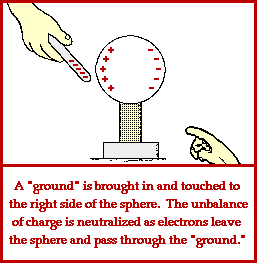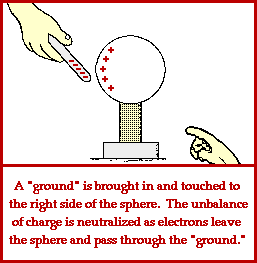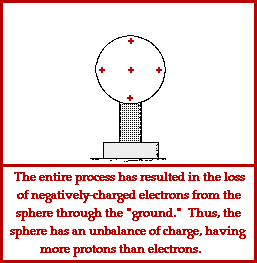
بعضی از اتم ها الکترون های خودشان را از دست داده اند. یک اتم که الکترون خود را از دست داده باشد، تعداد پروتون هایش بیشتر از الکترون ها و دارای بار مثبت است. یک اتم که الکترون بدست آورد ذرات منفی بیشتر و بار منفی دارد. یک اتم باردار یون نامیده می شود.
می توان الکترون ها را وادار کرد تا از یک اتم به اتم دیگر حرکت کنند. وقتی الکترون ها بین اتم ها حرکت می کنند، جریان الکتریسیته تشکیل می شود .
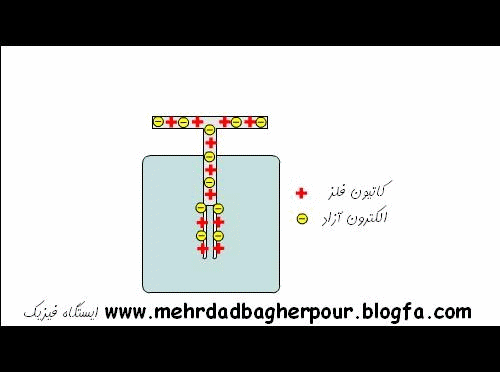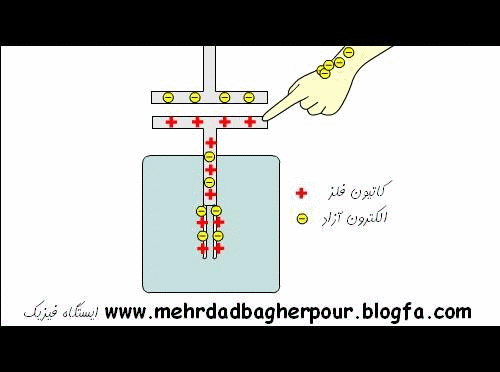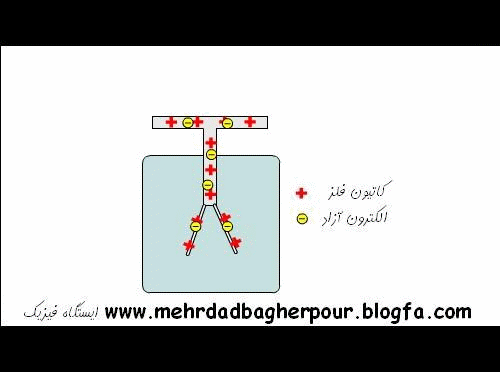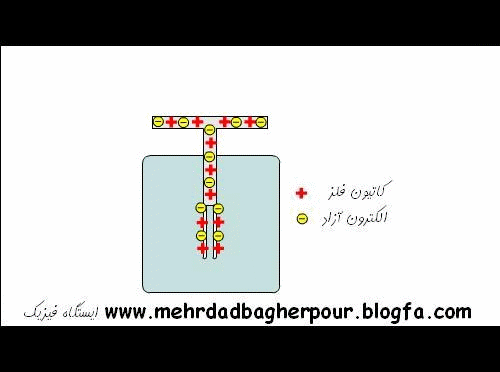
این زنجیره مانند خاموش کردن آتش بوسیله سطل در زمان های قدیم است. اما در این جا به جای منتقل کردن سطل از یک طرف به طرف دیگر ، هر شخص یک سطل دارد و فقط آب منتقل می شود (به این معنی که سطل خالی را به عنوان یون و سطل پر را به عنوان اتم خنثی و آب را به عنوان الکترون در نظر بگیریم. در رسانای فلزی یون ها منتقل نمی شوند بلکه الکترون ها منتقل می شوند) این کار خیلی به عبور جریان الکتریسیته شبیه است. در واقع بار از یک اتم به اتم دیگر منتقل می شود.
چون همه اتم ها دوست دارند در تعادل باشند. اتمی که نامتعادل شده است به دنبال الکترون آزادی می گردد تا جای خالی الکترون از دست رفته را پر کند. ما می گوییم که این اتم نامتعادل یک بار مثبت دارد چون تعداد زیادی پروتون دارد.
اما بار مثبت و منفی به الکتریسیته چه ربطی دارد؟
دانشمندان و مهندسان چندین راه برای تولید زیاد اتم مثبت و الکترون آزاد پیدا کرده اند. از آن جایی که اتم های مثبت دوست دارند تعادل داشته باشند، الکترون ها را به شدت جذب می کنند. الکترون ها نیز دوست دارند جزئی از یک اتم متعادل باشند، بنابراین آن ها نیز اتم های مثبت را جذب می کنند تا به تعادل برسند.
بنابر این هر چه اتم های مثبت یا الکترون های منفی بیشتری داشته باشید، جاذبه بین آن ها بیشتر است. چون بارهای مثبت و منفی، هم دیگر را جذب می کنند می توانیم کل جاذبه را "بار" بنامیم.
وقتی الکترون ها در بین اتم های ماده حرکت می کنند، یک جریان الکتریسیته تشکیل می شود. این چیزی است که در یک سیم اتفاق می افتد. الکترون ها از یک اتم به اتم دیگر منتقل شده و یک جریان الکتریکی از یک سر به سر دیگر بوجود می آید.
الکتریسیته در بعضی مواد بهتر از مواد دیگر منتقل می شوند. مقاومت یک ماده نشان می دهد که چقدر رسانای خوب جریان الکتریسیته است، هر چه مقاومت کمتر، رسانا بهتر. بعضی از مواد به شدت الکترون خود را نگه می دارند و الکترون ها در بین آن ها به سختی حرکت می کنند این مواد را عایق می نامیم. پلاستیک، لاستیک، لباس، شیشه و هوای خشک عایق های بسیار خوبی هستند و مقاومت بسیار بالا یی دارند.
مواد دیگری وجود دارند که الکترون های ضعیفی دارند، الکترون ها در بین آن ها به راحتی حرکت می کنند. این گونه مواد را رسانا گویند، اکثر فلزات مانند مس، آلومینیوم، یا استیل رساناهای خوبی هستند.
وقتی الکترون ها در بین اتم های ماده حرکت می کنند، یک جریان الکتریسیته تشکیل می شود.
کلمه الکتریسیته از کجا آمده است ؟
الکترون(Electrons)، الکتریسیته(electricity)، الکترونیک (electronic) و کلمات دیگری که با electr شروع می شوند از کلمه یونانی elecktor به معنی خورشید درخشان گرفته شده است. در یونان electron کلمه ای است که برای کهربا استفاده می شود.
کهربا سنگ قهوه ای طلایی بسیار زیبایی است که در نور خورشید برق نارنجی و زرد دارد. کهربا در واقع شیره فسیل شده درخت است. میلیون ها سال پیش حشرات در بین شیره درختان گیر افتادند. حشرات کوچکی که دایناسورها را نیش زده بودند در بدنشان خون با DNA دایناسورها است که حالا در کهربا فسیل شده است.
یونانی های قدیم کشف کردند که کهربا وقتی به خز یا اشیا دیگر مالیده می شود رفتار عجیبی از خود نشان می دهد. مانند جذب پر. آن ها نمی دانستند که چه چیزی باعث این پدیده می شود. اما آن ها یکی از مثال های الکتریسیته ساکن را کشف کردند.
کلمه لاتین الکتریک electricus به معنی تولید از کهربا بوسیله اصطکاک است.
بنابراین ما کلمه انگلیسی الکتریسیته electricity را از کلمات یونانی و لاتین که در مورد کهربا بود گرفته ایم.
| | نسخه قابل چاپ | تعداد بازديد : 45 |

نگاه کلی عناصر گروه اول جدول تناوبی که به فلزات قلیایی معروفند، در لایه ظرفیت الکترونی دارای آرایش ns1 هستند که n ، شماره دوره آنها است. آخرین عنصر به نام فرانسیم ، رادیواکتیو است که در اینجا مورد بحث قرار نمیگیرد. این عناصر ، فلزات نقرهفام رنگی هستند. آنها بسیار نرم بوده و به آسانی با چاقو بریده میشوند. سطح درخشان آنها در معرض هوا به علت اکسیداسیونکدر میشود.
این عناصر بشدت واکنش پذیر هستند. واکنش پذیری آنها از بالا به پایین گروه یعنی از Li به Cs افزایش مییابد و از این لحاظ شبیه عناصر سایر گروهها هستند. منابع فلزات قلیایی این فلزات بدلیل واکنشپذیری زیاد بطور آزاد در طبیعت یافت نمیشوند و معمولا بصورت ترکیب با سایر عناصر هستند. منبع اصلی سدیم ، هالیت یا Nacl است که بصورت محلول در آب دریا یا بصورت رسوب در بستر دریا یافت میشود. پتاسیم بصورت فراوان در اکثر معادن بصورت کانی سیلویت (Kcl) یافت میشود و همچنین از آب دریا هم استخراج میگردد.
فلزات قلیایی بسیار واکنشپذیر هستند و آنها را نمیتوان با جانشین کردن سایر فلزات بصورت آزاد تهیه کرد. فلزات قلیایی بصورت فلز آزاد را میتوان از الکترولیز نمکهای مذاب آنها تهیه کرد. خواص فیزیکی فلزات قلیایی از چند جهت با بقیه فلزات تفاوت دارند. آنها نرم بوده و دارای نقطه ذوب و نقطه جوش پایین هستند. دانسیته پایینی دارند، بطوریکه دانسیته K و Na و Li از دانسیته آب پایینتر است. آنتالپی استاندارد ذوب و تبخیر کمتری دارند. به علت داشتن فقط یک الکترون در لایه ظرفیت معمولا پیوندهای فلزی ضعیفی ایجاد میکنند. این فلزات وقتی در معرض شعله قرار میگیرند، رنگ آن را تغییر میدهند. وقتی عنصری در مقابل شعله قرار میگیرد، حرارت شعله انرژی کافی برای برانگیختن الکترون لایه ظرفیت را به لایههای بالاتر فراهم میکند.
الکترون در بازگشت به حالت پایه انرژی منتشر میکند و این انرژی دارای طول موج منطقه مرئی است که باعث میشود رنگ ایجاد شده در شعله دیده شود. شعاع یونی در فلزات قلیایی خاکی در مقایسه با شعاع اتمی آنها خیلی کوچکتر است. چون اتم یک الکترون در لایه S خود دارد که عدد کوانتومی آن با عدد کوانتومی لایه داخلی متفاوت است. بنابراین این لایه نسبتا دور از هسته است.
وقتی اتم این الکترون را از دست داده و به یون تبدیل میشود، الکترونهای باقیمانده در تراز نزدیک نسبت به هسته قرار دارند. بعلاوه افزایش بار مؤثر هسته آنها را بیشتر بطرف هسته جذب میکند. بنابراین اندازه یون کاهش مییابد. خواص شیمیایی
فلزات قلیایی عامل کاهنده قوی هستند. پتانسیل الکترود منفی آنها نشانگر میل شدید آنها برای از دست دادن الکترون در تبدیل به کاتیون در محلول است. آنها میتوانند اکسیژن ، کلر ، آمونیاک و هیدروژن را احیا کنند. در اثر واکنش با اکسیژن هوا اکسید شده و تیره میشوند. بنابراین در زیر نفت نگهداری میشوند. بعلت واکنش با آب و تولید هیدروژن و هیدروکسید قلیایی نمیتوان آنها را زیر آب نگهداری کرد.
از بالا به پایین ، به شدت واکنش با آب افزوده میشود. لیتیم به آرامی با آب واکنش داده و حبابهای هیدروژن آزاد میکند. سدیم بشدت و همراه با مشتعل شدن با آب واکنش نشان داده و با شعله نارنجی میسوزد. پتاسیم در اثر برخورد با آب به شدت مشتعل شده و با شعله بنفش میسوزد. سزیم در آب ته نشین شده و به سرعت تولید هیدروژن میکند. آزاد کردن هیدروژن همراه با ایجاد امواج ضربهای شدید است که میتواند باعث شکستن محفظه شیشهای شود.
Na در آمونیاک حل شده و ایجاد محلول آبی تیره میکند که بعنوان عامل کاهنده در واکنشها استفاده میشود. در غلظتهای بالا رنگ محلول برنزی شده و جریان الکتریکی را همانند فلز هدایت میکند.
چند مورد غیر عادی در شیمی Li دیده میشود. کوچک بودن اندازه کاتیون Li در نشان دادن خاصیت کووالانسی در برخی ترکیبات و ایجاد پیوند دیاگونالی با منیزیم از آن جمله است.
فلزات قلیایی در اثر واکنش با اکسیژن هوا ترکیب جامد یونی به فرمول  تولید میکنند. هر چند که Na غیر از این ، ترکیب پروکسید (
تولید میکنند. هر چند که Na غیر از این ، ترکیب پروکسید (  ) بعنوان فراورده عمده و پتاسیم هم سوپر اکسید (
) بعنوان فراورده عمده و پتاسیم هم سوپر اکسید (  ) را بطور عمده تولید میکند.
) را بطور عمده تولید میکند.
هیدروکسید فلزات قلیایی ، جامدات یونی به فرم کریستالی در رنگ سفید و فرمول MOH است. قابل حل در آب هستند و همه بجز LiOH آبدار میشوند. محلول آبی آنها باز قوی است. اسیدها را خنثی کرده و نمک تولید میکنند.
هالیدهاهالیدهای این فلزات ، همه جامد یونی به فرم کریستالی و به رنگ سفید بوده و قابل حل در آب هستند، جز LiF که بعلت داشتن انرژی شبکه بالا که ناشی از جاذبه الکتروستاتیکی بین یون کوچک +Li و -F است.
حالت اکسایشاین فلزات حالت اکسایش 0 و 1+ دارند. تمام ترکیبات شناخته شده آنها بر پایه +M است. اولین انرژی یونش آنها پایین است، زیرا الکترون آخرین لایه به خوبی الکترونهای لایه داخلی توسط جاذبه هسته محافظت نمیشود، بنابراین آسان تر برداشته میشود. انرژی دومین یونش بالا است، زیرا الکترون بعدی از لایه کامل برداشته میشود. همچنین بوسیله هسته ، بخوبی جذب میشود.انرژی یونیزاسیون از بالا به پایین با افزایش عدد اتمی و افزایش تعداد لایهها بعلت دور شدن الکترون ظرفیت از هسته کاهش مییابد.
اطلاعات صنعتیهیدروکسید ، کلرید و کربنات سدیم ، از جمله ترکیبات شیمیایی مهم صنعتی هستند. هیدروکسید سدیم از الکترولیز آب شور اشباع شده در پیل با کاتد فولادی و آند تیتانیوم تولید میشود. کربنات سدیم با فرآیند سالوی تهیه میشود. در این فرآیند کلرید سدیم قابل حل در آب به بیکربنات سدیم نامحلول تبدیل شده و بعد از صاف کردن و حرارت دادن به کربنات سدیم تبدیل میشود.
به هر حال محصول اصلی در این فرآیند کلرید کلسیم است و فرآیند رسوبگیری و حرارت و تهیه کربنات سدیم به کارخانه بستگی دارد. فرایند سالوی رفته رفته جای خود را به تهیه کربنات سدیم از جداسازی و تلخیص کربنات سدیم موجود به معادن میدهد.
| | نسخه قابل چاپ | تعداد بازديد : 49 |
هیدروژن تجاری در حجمهای زیاد معمولا بوسیله تجزیه گاز طبیعی تولید میشود.
هیدرودیلکیلاسیون (hydrodealkylation) ، هیدرودیسولفوریزاسیون (hydrodesulfurization) و هیدروکرکینک (hydrocracking) .
تولید اسید هیدروکلریک ، جوشکاری ، سوختهای موشک و احیاء سنگ معدن فلزی
هیدروژن مایع در تحقیقات سرما شناسی مانند مطالعات ابررسانایی بکار میرود
تریتیوم که در رآکتورهای اتمی تولید میشود، در ساخت بمبهای هیدروژنی مورد استفاده قرار میگیرد.
هیدروژن چهارده و نیم بار از هوا سبکتر است و سابقا بعنوان عامل بالا برنده در بالونها و کشتیهای هوایی مورد استفاده قرار میگرفت تا وقتیکه فاجعه هیندنبرگ ثابت کرد که استفاده از این گاز برای این منظور بسیار خطرناک است
دوتریوم بعنوان یک کند کننده جهت کاهش حرکت نوترونها در فعالیت های هستهای مورد استفاده قرار میگیرد و ترکیبات دوتریوم در شیمی و زیست شناسی در مطالعاتتاثیرات ایزوتوپ ، مورد استفاده واقع میشوند.
تریتیوم که یک ایزوتوپ طبقهبندی شده در علوم زیست شناسی است که بعنوان یک منبع تشعشع در رنگهای نورانی کاربرد دارد.هیدروژن میتواند در موتورهای درون سوز سوخته شود و در برهه کوتاهی اتومبیلهایی با سوخت هیدروژنی توسط شرکت Chrysler-BMW تولید شدند. پیل های سوختی هیدروژنی ، بعنوان راه کاری برای تولید توان بالقوه ارزان و بدون آلودگی ، مورد توجه قرار گرفته است.
هیدروژن سبکترین گازها با اکثر عناصر ترکیب شده و ترکیبات مختلف را بوجود میآورد. هیدروژن دارای عددالکترونگاتیویته 2.2 است، پس هیدروژن هنگامی ترکیبات را میسازد که عناصر غیر فلزیتر و عناصر فلزیتری وجود داشته باشند. در این حالت (غیر فلزی) تشکیل دهندهها هیدریدها نامیده میشوند که هیدروژن یا بصورت یونهای H- یا بصورت حل شده در عنصر دیگر وجود خواهد داشت (مانند هیدرید پالادیوم). در حالت دوم (ترکیب با فلز) هیدروژن تمایل برای تشکیل پیوند کووالانسی دارد، چون یونهای H+ بصورت یک اتم عریان فاقد الکترون در میآیند، بنابراین تمایل شدیدی به جذب الکترونها به سمت خود دارند. هر دوی اینها تولید اسید میکنند، لذا حتی در یک محلول اسیدی میتوان یونهایی مثل +H3O را دید که گویی پروتونها به جایی محکم به چیزی چسبیدهاند.هیدروژن با اکسیژن ترکیب شده ، تولید آب میکند، H2O که در این واکنش مقدار زیادی انرژی را بصورتی آزاد میکند که باعث انفجار در هوا میشود و یا به اکسید دوتریوم یا D2O که معمولا آب سنگین گفته میشود، تبدیل میشود. همچنین هیدروژن با کربن ترکیبات گسترده ای را بوجود می آورد. بخاطر ارتباط این ترکیبات با چیزهای زنده ، این ترکیبات را ترکیبات آلی مینامند و به مطالعه خصوصیات این ترکیبات ، شیمی آلی گفته میشود.
حالتها در شرایط عادی گاز هیدروژن ترکیبی از دو نوع متمایز مولکول است که با هم از نظر جهت چرخش الکترونها وهسته تفاوت دارند. این دو شکل به نام ارتو و پارا هیدروژن معروفند. در شرایط استاندارد ، هیدروژن معمولی ترکیبی از 25% شکل پارا و 75% شکل ارتو است. شکل ارتو را نمیتوان بصورت حالت خالص آن تهیه کرد. این دو مدل هیدروژن از نظر انرژی با هم متفاوتند که این مسئله موجب میگردد تا خصوصیات فیزیکی آنها کمی متفاوت باشد، مثلا نقطه ذوب و جوش پاراهیدروژن تقریبا 0.1K پائینتر از ارتوهیدروژن است. ایزوتوپهاپروتیوم ، معمولیترین ایزوتوپ هیدروژن فاقد نوترون است، گرچه دو ایزوتوپ دیگر به نام دوتریوم دارای یک نوترون و تریتیوم رادیواکتیویته دارای دو نوترون وجود دارند. دو ایزوتوپ پایدار هیدروژن پروتیوم(H-1) و دیتریوم(D ، H-2) میباشند. دیتریوم شامل 0.0184-0.0082% درصد کل هیدروژن است (IUPAC)؛ نسبتهای دیتریوم به پروتیوم با توجه به استاندارد مرجع آب VSMOW اعلام میگردد. تریتیوم(T یا H-3) یک ایزوتوپ رادیواکتیو دارای یک پرتون و دو نوترون میباشد. هیدروژن تنها عنصری است که ایزوتوپهای آن اسمهای مختلفی دارند.
هشدارها هیدروژن ، گازی است با قدرت اشتعال فوقالعاده زیاد. این گاز همچنین بهشدت با کلر و فلوئور واکنش نشان میدهد. D2O یا آب سنگین برای بسیاری از گونهها سمی است. اما مقدار قابل توجهی از آن برای کشتن انسان لازم است.| | نسخه قابل چاپ | تعداد بازديد : 31 |
ارنست رادرفورد مدل اتمی خود را در آغاز دههی 1910 ارائه کرد. در مدل رادرفورد بارهای مثبت در هستهی اتم جمع شدهاند و الکترونها در اطراف هسته در گردشاند.
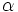 را بر ورقه نازک طلا تابش داد، هم نظریه اتمی قدیمی دالتون و هم نظریه استاد خود، تامسون را رد کرد. آزمایشات نشان میداد که اغلب ذرات آلفا (9/99 %) بدون انحراف، در مسیر اصلی خود از درون ورقه طلا عبور میکنند، این پدیده میرساند که قسمت اعظم درون اتم را فضای خالی تشکیل میدهد. این آزمایش همچنین نشان میدهد که از میان تعداد بسیار زیاد ذرههای آلفا، تعداد بسیار کمی (مثلاً به نسبت 1 به 8000) به عقب برمیگردند.
را بر ورقه نازک طلا تابش داد، هم نظریه اتمی قدیمی دالتون و هم نظریه استاد خود، تامسون را رد کرد. آزمایشات نشان میداد که اغلب ذرات آلفا (9/99 %) بدون انحراف، در مسیر اصلی خود از درون ورقه طلا عبور میکنند، این پدیده میرساند که قسمت اعظم درون اتم را فضای خالی تشکیل میدهد. این آزمایش همچنین نشان میدهد که از میان تعداد بسیار زیاد ذرههای آلفا، تعداد بسیار کمی (مثلاً به نسبت 1 به 8000) به عقب برمیگردند.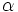 را با پخش یکنواخت ذرات مثبت و منفی در اتم به هیچ وجه نمیتوان توجیه کرد.
را با پخش یکنواخت ذرات مثبت و منفی در اتم به هیچ وجه نمیتوان توجیه کرد.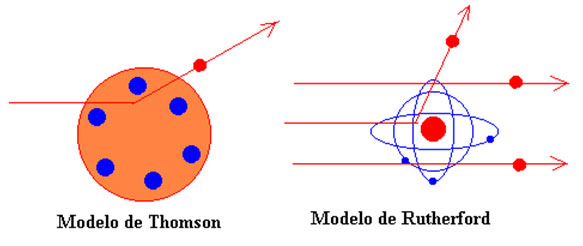
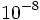 و شعاع هسته
و شعاع هسته 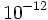 سانتیمتر تخمین زده شد از این نسبت متوجه میشویم که اتم در واقع توخالی میباشد، تصور مقیاسی از این مدل حائز اهمیت است. اگر هسته اتم به اندازه یک توپ تنیس باشد، قطر اتم بیشتر از 5/1 کیلومتر خواهد بود.
سانتیمتر تخمین زده شد از این نسبت متوجه میشویم که اتم در واقع توخالی میباشد، تصور مقیاسی از این مدل حائز اهمیت است. اگر هسته اتم به اندازه یک توپ تنیس باشد، قطر اتم بیشتر از 5/1 کیلومتر خواهد بود.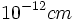 و الکترونها در خارج هسته در قشرهایی به شعاع نهایی
و الکترونها در خارج هسته در قشرهایی به شعاع نهایی 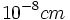 بر روی مدارهایی قرار دارند. معذلک این ساختمان اتمی، خالی از اشکال نبود و بنا به کلیه اصول فیزیک کلاسیک (1911) اتم میبایستی ناپایدار باشد. زیرا اگر الکترونها در روی قشر بخصوصی مستقر باشند. هیچگونه مانعی برای جذب آنها به هسته وجود ندارد و نیز اگر متحرک باشند، بر طبق قوانین الکترومغناطیس مادامی که الکترونها در حال حرکت هستند. اتم میبایستی از خود نور منتشر سازد.
بر روی مدارهایی قرار دارند. معذلک این ساختمان اتمی، خالی از اشکال نبود و بنا به کلیه اصول فیزیک کلاسیک (1911) اتم میبایستی ناپایدار باشد. زیرا اگر الکترونها در روی قشر بخصوصی مستقر باشند. هیچگونه مانعی برای جذب آنها به هسته وجود ندارد و نیز اگر متحرک باشند، بر طبق قوانین الکترومغناطیس مادامی که الکترونها در حال حرکت هستند. اتم میبایستی از خود نور منتشر سازد.منبع : سایت رشد
| | نسخه قابل چاپ | تعداد بازديد : 164 |
الکترونی که از اتم جدا شده و به آن وابستگی ندارد، الکترون آزاد خوانده میشود.. الکترونهای بیرونیترین لایههای اتم فلزات بستگی کمتری نسبت به اتمهای خود دارند و با کمترین انرژی از این اتمها کنده میشوند و به شکل تودهای از ابر یا گاز ، شبکههای اتمی فلزات را در بر میگیرند. هنگامی که الکترونهای آزاد در میدان الکتریکی قرار گیرند، جریان الکتریکی بوجود میآید.

سیر تحولی و رشد
در سالهای پایانی سده نوزدهم میلادی ، بیشتر فیزیکدانان به این باور رسیدند که الکتریسته به دو صورت ظاهر میشود: یکی به صورت الکترون با جرم 9.109534X10-31 kg و بار منفی 1.602177X10-19 C- و دیگری به صورت پروتون با جرم 1.672623X19-27 kg و بار مثبت 1.602177X10-19 C .
اعتقاد بر این بود که اتمها (و در نتیجه مولکولها) از ترکیب الکترونها و پروتونها مشکل میگیرند.
در اوایل 1930 معلول شد که هسته اتمها ( بجز اتم هیدروژن ) از پروتونهای مثبت و نوترونهای خنثی ، با جرم 1.675X10-27 و بدون بار الکتریکی ، تشکیل میشود. همچنین کشف شد که الکترون مثبت نیز با جرمی برابر با جرم الکترون و باری برابر با بار الکترون ولی با علامت مثبت (دست کم به صورت لحظهای) وجود دارد.
اتم الکترون اوژه ، نوعی الکترون آزاد است که از اتم یا یون گسیل میشود. الکترون اوژه از بازآیی الکترونهای مقید در اتم یا یون اولیه سرچشمه میگیرد. این بازآیی از طریق برهمکنش الکترون - الکترون ، که مولد نیروی دافعه است و میتواند بر نیروی جاذبه ناشی از برهمکنش الکترون - هسته فائق آید، صورت میگیرد. با این همه ، بازآیی یاد شده تنها هنگامی میتواند رخ بدهد که حداقل یک الکترون در تراز انرژی همین اتم یا یون اولیه خالی باشد و در تراز با انرژی بیشتر از انرژی تهی جا حداقل دو الکترون وجود داشته باشد.
یکی از الکترونهای تراز بالاتر به تراز دارای تهی جا سقوط میکند و الکترون دیگر بهصورت الکترون آزاد از اتم خارج میشود. بنا بر پایستگی انرژی ، اوژه گسیل شده انرژی جنبشی معینی دارد که برابر است با انرژی بستگی کل اتم یا یون در حالت اولیه منهای انرژی بستگی کل در حالت نهایی.
رساناونارسانا
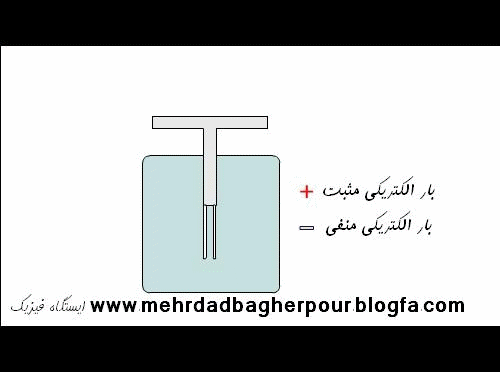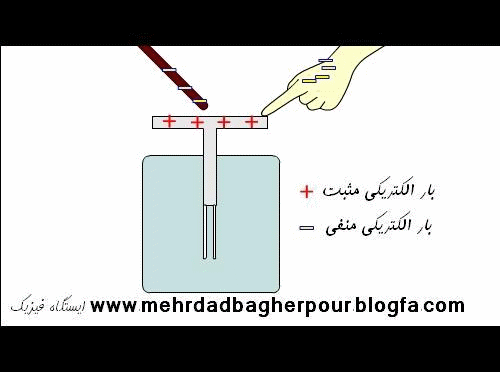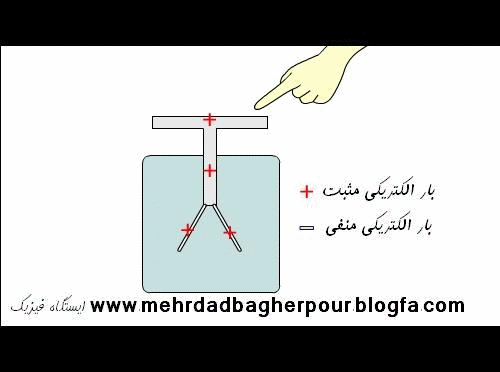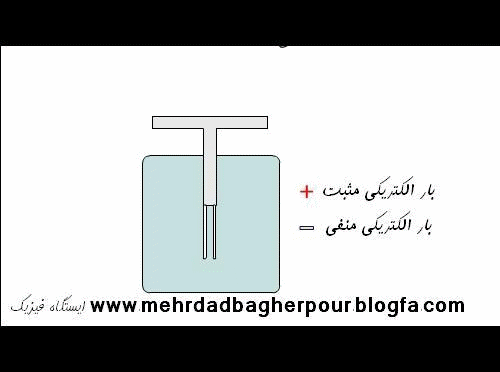
برای درک درست تفاوت اجسام رسانا و اجسام نارسانا(عایق) از دیگاه اتمی ، به شکل های زیر و توشته های آنها به دقت توجه کنید.
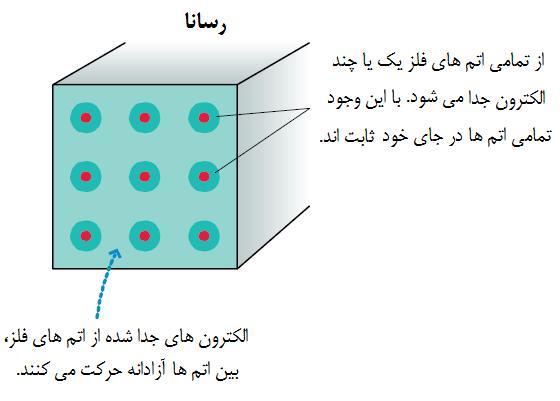
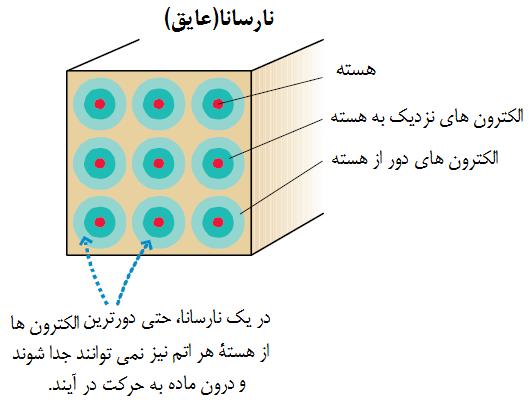
منبع: سایت رشد
| | نسخه قابل چاپ | تعداد بازديد : 219 |
وقتی که ستاره ای منبع سوخت هیدروژن هسته اش را به پایان برد بسته به جرمش به غول یا ابرغول تبدیل می شود.
بعد از اتمام هیدروژن هسته ,همجوشی هیدروژن برای تولید هلیوم متوقف می شود وهسته شروع به انقباض می کند .با انقباض هسته انرژی آزاد می شود واین انرژی موجب شروع واکنش در هیدروژن لایه های بالایی می شود .بنابراین واکنشهای هسته ای از مرکز به لایه های بالاتر منتقل می شود به دنبال آن لایه های بیرونی ترهیدروژنی انرژی را جذب کرده ومتورم می شوند(در نظر داشته باشیدکه این انرژی به سمت لایه های زیرین وهسته کشیده نمی شود بلکه تمایل آن به رسیدن به مناطق سرد بیرونی تر است) در این مرحله ستاره از رشته اصلی جدا شده و وارد مرحله زیر غولی وسپس مرحله غولی ودر صورت پرجرم بودن وارد فاز ابرغولی میشود .
دمای متوسط غولها بین 2000 تا 4000 درجه کلوین شده ورنگ شان نیز به قرمزی می گراید.این ستاره هااز رده طیفی M یا K بوده ودر منطقه بالا سمت راست در نمودار هرتسپرونگ راسل قرار دارند.
همانطور که از نمودار آشکار است با گذشت زمان دمای این ستاره ها تقریبا ثایت مانده ولی درخشندگی شان افزایش می یابد.این نشان دهنده افزایش انرژی برونداد آنهاست .با توجه به اینکه دمای نسبتا ثابتی دارند افزایش انرژی برونداد نشان دهنده این است که مساحتشان و در واقع قطرشان در این مرحله باید زیاد شود(و غول شوند).
قطر این ستاره ها بین ده تا هزار برابر خورشید است.اگر جرم ستاره اولیه از 8 برابر جرم خورشید کمتر باشد به یک غول واگر از 8برابر جرم خورشید سنگین تر باشد به یک ابرغول تبدیل خواهد شد.عمر یک غول یا ابرغول درحدود یکدهم عمر آن در حالت گذران رشته اصلی می باشد.غولها از ستاره هم دمای خود دررشته اصلی بسیاردرخشنده ترند. این ستاره ها معمولا"متغییر بوده(در این مرحله با نام متغییرهای قیفاووسی شناخته می شوند) ولایه های سطحی آنها دارای تپش می باشد.بدلیل قطر زیاد آنها نیروی گرانش در لایه های سطحی آن کم شده ومعمولا" به شکل باد ستاره ای مواد از آن فرار کرده و سحابی سیاره ای تشکیل می دهند.
خورشید خودمان بعد از تبدیل شدن به غول سرخ با اندازه حدود 60 درجه وبا رنگ قرمز تیره در آسمان دیده خواهد شد.ستاره سماک رامح والدبران دو نمونه از ستاره های گونه غول سرخ هستند.
ماهواره ستاره شناسی مادون قرمز IRIS تاکنون تعداد زیادی غول قرمز کشف کرده که درون پوسته ای از گاز وغبار قرار دارند این ستاره ها بادمای چندصد درجه تنها در امواج مادون قرمز قابل کشف هستند.
| | نسخه قابل چاپ | تعداد بازديد : 35 |

یک انفجار ستاره ای که در آن کل ستاره تحت تاثیر قرار می گیرد. بدنبال انفجارنورانیت ستاره حتی به اندازه 20 قدر می تواند درخشانتر شود.ابرنواخترها با توجه به بودن یا نبودن هیدروژن در طیفشان به دو دسته یعنی ابرنواختر نوع یک ونوع دو تقسیم می شوند.ابرنواخترهای نوع یک
(Type I) نشانی از وجود هیدروژن در طیفشان ندارند در حالیکه ابرنواخترهای نوع دو(Type II) دارند.در حال حاضر می دانیم که دلیل اصلی انفجار بودن یانبودن هیدروژن نیست بنابراین دسته بندیهای جدیدی تعریف شده اند.دومدل برای توجیه انفجار وجود دارد.
مدلهای توجیه انفجار
در مدل اول٬ ابرنواخترهای با هسته رمبنده می باشند که در حقیقت ستاره های پرجرمی هستند که سوخت هسته ای درونشان به اتمام رسیده است و با توجه به اینکه جرم هسته به ماوراء حد چاندراسخار یعنی بسیار بیشتر از ۴۴/۱ برابر جرم خورشید میرسد انقباض هسته تا رسیدن به فشار دژنره نوترونی ودر واقع تبدیل شدن ستاره به یک ستاره نوترونی ادامه پیدا می کند ودر نتیجه این وضعیت مواد ستاره در لایه های بالایی جو به شکل انفجار مهیب به بیرون پرتاب می شوند.
در مدل دوم انفجار ابرنواختری در ستاره های دوتایی بسیار نزدیک رخ می دهد که در آن جرم ستاره کوتوله سفید بدلیل جاری شدن مواد از ستاره همدم به سوی آن از حد چاندراسخار بیشتر می شود وستاره کوتوله سفید به حالت انفجار می رسد وابرنواختر بوجود می آید.
ستارگان در حالیکه چرخه تکاملی ستاره خود را طی میکنند درون هسته اشان به تدریج عناصر سنگین(عناصر هلیم ،کربن ،.........الی آهن) تولید می شود ولی بدنبال انفجار ابرنواختری معمولا"تمام عنصرهای جدول تناوبی، بخصوص عنصرهای سنگینتر از آهن که در شرایط عادی تولید نمیشوند، تشکیل می شوند.برای تولید این عناصر سنگینتر تنها یک انفجار هسته ای مخرب وپرانرژی است که می تواند دما وفشار لازم را تولید کند.
انواع ابرنواخترها
ابرنواخترهای نوع یک که خود شامل چند زیر گروه می باشد.
۱ - زیر گروه Ia در تمام کهکشانها وجود دارند اما در بازوهای مارپیچی کهکشانهای مارپیچی کمتر به چشم می خورند.این ابرنواخترها دارای عناصری مانند منیزیم٬ سیلیکون٬ گوگرد وکلسیم هستند که در زمان حداکثر نورانیت در طیف آشکار می شوند وبعد ازگذشتن از حال حداکثر نورانیت با کاهش نور٬ آهن نیز خودنمایی می کند.نمودار نور این گونه ابرنواخترها طی حدود دوهفته افزایش نورانیت را نشان می دهد وپس از آن با کاهش نورانیت طی چند ماه روبرو می شود.تصور براین است که ابرنواخترهای نوع Ia ناشی از انفجار بدلیل انتقال جرم بین ستاره ای پیر باعمر زیاد در یک ستاره دوتایی بسیار نزدیک بهم باشد.از آنجاییکه درخشندگی این ابرنواخترها زیاد است از آنها برای تخمین فاصله کهکشانهای بسیار دور استفاده می شود.
۲- ابرنواخترهای زیر گروه Ib و Ic که فقط در بازوهای کهکشانهای مارپیچی رخ می دهند.هر دو گونه نشانهایی از اکسیژن منیزیم وکلسیم بعد از حداکثر نورانیت در طیفشان دارند.علاوه بر آن ابرنواخترهای گونه Ib در نزدیکی حداکثر نورانیت نشانهایی از وجود هلیم در طیفشان دارند.منحنی نوری هر دو گونه Ib وIc مانند گونه Ia می باشد با این تفاوت که در زمان حداکثر نورانیت نور آنها کمتر از نور ابرنواخترهای گونه Ia می شود .دوگونه IbوIcمعمولا"چشمه امواج رادیویی هم می باشند در حالیکه ابرنواخترهای Ia دارای چنین خاصیتی نیستند.تصور براین است که ابرنواخترهای گونه Ib و Ic ناشی از انفجار در ستارگان پرجرمی باشند که محتوی هیدروژنی شان به اتمام رسیده ودر گونه Ic محتوی هلیومی نیز به اتمام رسیده باشد.
ابرنواخترهای نوع II در کهکشانهای بیضوی بچشم نمی خورند بجای آن در بازوهای کهکشانهای مارپیچی وگاهی در کهکشانهای نامنظم بچشم می خورند.این ابرنواخترها طیف معمولی مانند بقیه ستاره ها از خود نشان می دهند.منحنی نور این ابرنواختر ها طی حدود یک هفته به حداکثر می رسد برای حدود یک ماه تقریبا" ثابت می ماند وسپس طی چند هفته ناگهان کاهش می یابد وطی چند ماه در همین وضعیت با نور ناچیز باقی می ماند.تصور براین است که این گونه ابرنواخترها نتیجه انفجار در هسته یک غول سرخ با یک گستره پرجرم باشند.
بدنبال انفجار ابرنواختری یک ستاره نوترونی بوجودمی آید که احتمال دارد در مرکز پوششی کروی از ابرباشد که این ابر همان مواد ستاره است که به بیرون پرتاب شده است.این ابر یا سحابی ٬باقیمانده ابرنواختری(supernova remanent) نام دارد.باقیمانده های ابرنواختری که یک تپنده در میان آن باشد PLERION نامیده میشود.آهنگ مشاهده ابرنواختر در یک کهکشان معمولی در حدود یک ابرنواختر در صد سال است ودر کهکشانهایی که از لبه دیده می شوند بدلیل غبارهای تیره کننده بسیارکم هستند.در هزاره گذشته تنها پنج ابرنواختر در کهکشان راه شیری مشاهده شده است بعلاوه ابرنواختر SN 1987 که در ابر ماژلانی که احتمالا یک کهکشان قمر کهکشان راه شیری می باشد. با آمدن فن آوری CCD به میان ستاره شناسان آماتور همواره برتعداد ابرنواخترهایی که در دیگر کهکشانها کشف می شوند افزوده شده است.تلسکوپهای خودکار نیز که با هدایت کامپیوتر بطور اتوماتیک به عکسبرداری ومقایسه عکسها از هزاران کهکشان طی یک شب می پردازند کمک بزرگی به کشف ابرنواخترها کرده اند.
ابرنواختر سال 1054 بعنوان منشاء سحابی خرچنگ در صورت فلکی ثور توسط ادوین هابل معرفی شده است.مانند دوابرنواختر سال 1006 و1181 این ابرنواختر توسط ستاره شناسانی از مشرق زمین ثبت شده بودند.ستاره شناسانی از چین ٬کره٬ مسلمانان واروپاییان در ثبت این ابرنواخترها سهم داشته اند.نشانهایی از ابرنواختر سال 1054 در نقاشیهایی در قاره آمریکا به چشم می خورد.
ابرنواختر سال 1572 بادقت توسط تیکوبراهه رصد شده است.او به ثبت موقعیت وتغییرات نورانیت آن بطور روزانه پرداخت.اومتوجه شد که باوجود چرخش زمین هیچ اختلاف منظری وجود ندارد بنابراین این جرم باید ماوراء مدار ماه باشد.حرکت نکردن این جرم طی 18 ماه که ناپدید شد نشان می داد که مدار آن باید ماوراءمدار زحل باشد(در آن زمان دورترین سیاره شناخته شده زحل بود).این مشاهدات آنرا در میان بقیه ستارگان آسمان قرار داد.ابرنواختر سال 1604 بانام ستاره کپلر شناخته می شود گرچه او اولین نفری نبود که آنرا مشاهده می کرد.نشانه هایی وجود دارد که در سال 1680 نیز ابرنواختری در صورت فلکی ذات الکرسی وجود داشته است.توده ابری بزرگ ودر حال گسترش در این منطقه وجود دارد که دارای تابش قوی امواج رادیویی نیز می باشداین سحابی بانام ذات الکرسی A شناخته می شود.هیچ انفجار نوری از این انفجار گزارش نشده است.امکان دارد ستاره قبل از انفجار لایه های بیرونی خود را پرتاب کرده باشد یا اینکه انفجار آن ضعیف بوده است ستاره شناسان بکمک تلسکوپ فضایی هابل شاهد چگونگی تحول باقیمانده یک انفجار ابر نواختری در ابر بزرگ ماژلانی در نیمکره جنوبی آسمان هستند.این انفجار در سال 1987 میلادی رخ داد واکنون با نام باقیمانده ابر نواختری 1987A بعنوان نزدیک ترین ابرنواختر 400 سال اخیر شناخته می شود.نزدیکی این انفجار به دانشمندان اجازه داده تا چگونگی تحول آن را پیگیری نمایند.طبق مشاهدات جدید باقیمانده این انفجار که طی سالهای گذشته در حال کم نور شدن بود در حال پرنور شدن است.به نظر می رسد که فرایندی جدید موجب دادن انرژی به این ابرهای باقیمانده از انفجار باشد.ابرهای ناشی از انفجار در حال برخورد با حلقه های باقیمانده سرد تر که قبلا" در اطراف ستاره وجود داشته اند هستند ودر طی این برخوردها امواج شوکی قوی ایجاد شده که خود عامل تشکیل پرتوهای قوی مشاهده شده در ناحیه اشعه ایکس می باشد واین امواج توسط تلسکوپ اشعه ایکس چاندرا قابل مشاهده می باشند.
این امواج اشعه ایکس با ابرهای ناشی از انفجار ابرنواختر برخورد داشته وموجب درخشندگی آنها در ناحیه دیدگانی طیف می شوند.
منبع: دانشنامه ستاره شناسی
| | نسخه قابل چاپ | تعداد بازديد : 44 |
فرض کنید جرم ستاره ای درحدود 20 برابر جرم خورشید باشد بعد از طی مراحل تکامل وانفجار بصورت ابرنواختری, اگر جرم ستاره باقی مانده به سه برابر خورشید برسد از آنجاییکه این جرم برای تبدیل به ستاره نوترونی شدن زیاداست ستاره بطور کامل متراکم شده و به یک سیاهچاله تبدیل خواهد شد.برطبق قوانین فیزیک واستنتاج منطقی عاقبت کار یکتایی (Singularity) خواهد بود.یکتایی نقطه ای که شعاع آن صفر وچگالی آن بینهایت خواهد بود.هر چه به این جرم نزدیکتر شویم سرعت فرار از آن بیشتر خواهد شد و در فاصله ای که بانام شعاع شوارزشیلد شناخته میشود سرعت فرار از چنین جرمی با سرعت نور برابر می شود.اندازه این شعاع ویژه به جرم ستاره بستگی مستقیم دارد برای ستاره ای با جرم خورشید مقدار آن 3 کیلومتر است این بدان معناست برای اینکه خورشید به یک سیاه چاله تبدیل شود باید قطر آن به 3 کیلومتر کاهش بیابد.اگر کره ای با شعاع شوارزشیلد حول نقطه مرکزی رسم کنیم (نام این کره افق رویداد(Event horizon )می باشد)درون این کره سرعت فرار از سرعت نور بیشتر خواهد بود و از آنجاییکه هیچ جسمی توانایی حرکت باسرعت بیشتر از سرعت نور را ندارد ، هیچ جسمی توانایی گریز از این منطقه را ندارد.برطبق روابط فیزیکی معمول هیچ خبری از درون این کره در دسترس نمی باشد و نیروهای شدید کشندی درون این محیط موجب انفجار و از هم گسیختگی هر جسمی که به آن نزدیک شود می گردد.
برطبق نسبیت عام فضای اطراف افق رویداد به شدت تاب برمی دارد.مقدار تاب برداشتن به جرم سیاهچاله بستگی دارد وهر جرم بیشتر باشد مقدار آن بیشتر خواهد بود.از آنجاییکه سیاه چاله هیچ نوری از خود بیرون نمی دهد تنها براساس همین تغییر فضای اطراف آن است که ما می توانیم وجود آنرا بطور غیرمستقیم ردیابی کنیم.درواقع مابا مشاهده اثر آن بر مواد بیرون از افق رویداد میتوانیم تاحدودی آنرا تشخیص دهیم.سیاهچاله مواداطراف خود را به شدت جذب می کند واین مواد جذبی قبل از برخورد با آن به دلیل سرعت سقوط فوق العاده زیاد پرتوهای ایکس گاما و امواج رادیویی گسیل می کنند.
سیاهچاله هایی که در یک دستگاه دوتایی قرار دارند از گازهای ستاره همدم خود گازدریافت می کنند واین گاز با نزدیک شدن به افق رویداد دراثر نیروهای شدید گرانشی گرم شده وشروع به تابش اشعه ایکس می کنند پس یک راه برای تشخیص سیاهچاله ها جستجوبرای یافتن ستاره های دوتایی است که منبع قوی امواج اشعه ایکس باشند.موادی که از ستاره همدم می آیند بطور مستقیم برسطح سیاهچاله سقوط نمی کنند بلکه ابتداتشکیل یک قرص برافزایشی می دهند مواد درون این قرص با حرکت سریع ومارپیچی به سیاهچاله نزدیک شده وبه مرور زمان میسوزند.عکسهای گرفته شده توسط تلسکوپ فضایی هابل در مواردبسیار زیادی نشاندهنده این قرص می باشد.
این گمان وجود دارد که در مرکز کهکشانها سیاهچاله های ابر سنگین وجود داشته باشد.از جمله در کهکشان خودمان.نحوه حرکت ابرهای گازی وشدت پرتوهای ارسالی از مرکز کهکشان خودمان از دلایل وجود چنین سیاهچاله ای می باشد. بررسی سرعت ستارههای نزدیک به مرکز کهکشان راه شیری که امروزه توسط تلسکوپهابل قابل انجام است، بیانگر این واقعیت است که جرم هسته کهکشان بسیار بزرگ بوده که در یک ناحیه کوچک قرار دارد این نمونه میتواند وجود سیاهچاله در مرکز کهکشانها را مورد تایید قرار دهد. همچنین مشاهده اشعه گاما متغییر را میتوان به عنوان شاهدی دال بر قبول سیاهچاله ابرجرمدار در مرکز کهکشانها دانست. اخیرا" وجود سیاهچاله در مرکز کهشکان M87 نیز مورد قبول منجمین قرار گرفته است.
چگالی متوسط یک سیاهچاله متناسب با عکس مربع جرم آن است. برای یک سیاهچاله در حد جرم خورشید چگالی ده میلیون تن در سانتی مترمکعب بدست میآید که چهل برابر چگالتر از مواد هستهای است . در صورتی که برای یک سیاهچاله با جرم صد میلیون برابر جرم خورشید چگالی یک گرم در سانتی مترمکعب محاسبه میشود که برابر چگالی آب است. بنابراین شرایطی که میتواند یک سیاهچاله کوچک ایجاد گردد بسیار سخت تر از شرایطی است که یک سیاهچاله بزرگ میتواند تولید شود.
بطورکلی سیاهچاله ها به سه گروه تقسیم می شوند:
سیاهچالههای ستارهای (Stellar Black Holes )
این دسته از سیاهچالهها معمولا" از رمبش ستارگان بوجود آمده و جرم آنها بین 3 تا 100 برابر جرم خورشید است. بهترین کاندید برای مشاهده این دسته از سیاهچالهها، سیستمهای دوتایی منبع اشعه X است که یکی از دو شی مشاهده نمیشود. این دسته از سیستمهای نجومی از خود اشعه X تشعشع میکنند که از اوایل دهه 1970 مورد توجه قرار گرفتند.
اولین دوتایی کاندید از این گروه، Cygnus X-1 است که ستاره اپتیکی دوتایی یک ابرغول آبی است که جرم آن حدود 20 برابر جرم خورشید است و دور زوج نامرئی خود که جرم آن در حدود 40 برابر جرم خورشید است با پریود 6/5 روز میچرخد. فاصله آن از ما در حدود 2/2 کیلو پارسک است . در این سیستم دوتایی، جرم از ستاره قابل رویت دوتایی به درون سیاهچاله وارد میشود ولی به دلیل سرعت زاویهای، این جرم به صورت شعاعی وارد سیاهچاله نشده بلکه گازها تشکیل یک دیسک داده که آنرا قرص برافزایشی (accretion disk) گویند.
دو دسته اشعه در طیف تابش این سیستم دوتایی که از قرص برافزایشی تابش میگردد دیده میشود که یکی از این دو، تابش جسم سیاه با دمای 31000K بوده و دسته دوم اشعه X سخت تا انرژی 150K است . در واقع طیف این دسته دوم اشعه که تا انرژی 150Kev را هم داراست شاهدی بر وجود سیاهچاله بعنوان زوج نامرئی این دوتایی است. البته اگر این زوج ستاره نوترونی هم باشد اشعه X تولید میشود ولی نشان داده شده است که در این صورت اشعه X دارای انرژی حدود100K نخواهد بود . اخیرا" اشعه گاما پرانرژی هم برای این دوتایی مشاهده شده است که بر سیاهچاله بودن شی غیرقابل رویت این دوتایی تاکید میکند. تا کنون تعداد زیادی از این سیستمهای دوتایی که میتواند شاهد وجود سیاهچاله باشد کشف شده است و امروزه یکی از زمینههای مشاهدهای کشف و بررسی این گونه دوتاییهاست.
2-سیاهچالههای ابرجرم دار (Supermassive Black Holes )
جرم اینگونه سیاهچاله بین یک میلیون تا ده هزار میلیون برابر جرم خورشید است. اینگونه سیاهچالهها در مرکز کهکشانها از جمله کهکشان راه شیری قرار دارند. شدت تابش از مرکز کهکشانهای فعال که میتواند به خاطر ورود جرم به مرکز کهکشان باشد و کوچک بودن اندازه هسته این کهکشانها بیانگر وجود سیاهچاله ابرجرم دار در مرکز آنهاست.
3- سیاهچالهها با جرم متوسط
شکاف بین جرم سیاهچالههای معمولی (3 تا 100 برابر جرم خورشید) و سیاهچالههای ابرجرمدار (با جرم یک میلیون تا ده هزار میلیون برابر جرم خورشید) منجمین را بر آن داشت که به دنبال سیاهچالههایی با جرم(با جرم 100 تا 100هزار برابر جرم خورشید) هم باشند. این گونه سیاهچالهها میتوانند در مرکز خوشههای ستارهای در نزدیکی مرکز کهکشانها وجود داشته باشند. به دو روش میتوان به دنبال شواهد تجربی برای این دسته از سیاهچالهها بود. یکی از روشهای مشاهدهای این گونه سیاهچالهها یافتن منابع اشعه با شدت زیاد است. اخیرا" منابعی از اشعه X با این محدوده شدت با طیف انرژی چند ده الکترون ولت در مرکز خوشههای ستارهای مشاهده شده است. این دسته از منابع اشعه به منبع فوق درخشان پرتو ایکس یا Ultraluminous X-ray source (ULXs)مشهور هستند.
کلمه سیاهچاله از اینجا گرفته شده که هیچ پرتوی الکترومغناطیسی نمی تواند از آن ساطع شود درنتیجه سیاه دیده میشود.
منبع: با اقتباس از مقاله ای از دکتردهقانی از دانشگاه شیراز
آیا سیاهچاله همیشه سیاهچاله باقی میماند، یا به چیز دیگری تبدیل میشود؟
جسمی که سیاهچاله شد، دیگر تا ابد سیاهچاله خواهد بود. تنها تغییر مهمی که میتواند در سیاهچاله رخ بدهد، افزایش یافتن جرم آن بر اثر بلعیدن مواد مختلف است (شاید از ستارهی نزدیکش، یا از گازهای مرکز کهکشان و یا فضانورد بختبرگشتهای که زیادی به آن نزدیک شده است!).
از دید نظری، سیاهچاله میتواند تبخیر شود. این موضوعی است که نخستین بار استفان هاوکینگ به آن پی برد. پدیدههایی در عرصهی مکانیک کوانتومی وجود دارند که میتوانند باعث شوند که سیاهچاله پرتوهایی از خود گسیل کند. همین موضوع باعث میشود که سیاهچاله انرژی از دست بدهد و بنابر فرضیهی اینشتین، از دست دادن انرژی معادل است با کاهش جرم.
پس سیاهچاله میتواند لاغر هم بشود. البته این تابش هاوکینگ بسیار ضعیف است. به عنوان مثال، سیاهچالهای که به اندازهی خورشید جرم داشته باشد، 1067 سال طول میکشد تا تبخیر شود. این مقدار بسیار بیشتر از عمر کنونی عالم است. تازه، سیاهچالههای سنگینتر، بسیار دیرتر از این تبخیر خواهند شد. سیاهچالهی مرکزی کهکشان ما، که بین 3 تا 4 میلیون برابر خورشید جرم دارد، بیشتر از یک میلیارد میلیارد برابر دیرتر تبخیر میشود.
منبع: دانشنامه ستاره شناسی
| | نسخه قابل چاپ | تعداد بازديد : 36 |
آب سنگین آبی است که هیدروژن های آن، دوتریوم (ایزوتوپ سنگین هیدروژن) است. این آب در مقایسه با آب معمولی دیرتر می جوشد و زودتر یخ می زند و گیلبرت وییس نخستین بار نمونه آن را از آب سنگین خالص در سال 1933 به دست آورد. هیدروژن طبیعی دارای دو ایزوتوپ است. ایزوتوپ هیدروژن سبک تقریبا٩٨/٩٩ درصد هیدروژن موجود را تشکیل می دهد. ایزوتوپ دوتریوم برخلاف هیدروژن عمومی دارای یک نوترون است.
آب معمولی از یک اتم اکسیژن و دو اتم هیدروژن تشکیل شده است. در حالی که آب سنگین، از یک اتم اکسیژن و دو اتم دوتریوم(D) تشکیل شده است. برای تولید آب سنگین باید مولکول های آب حاوی هیدروژن سنگین (دوتریوم) را ازمولکول های آب معمولی جدا کنند یا از داخل هیدروژن، اتم های هیدروژن سنگین یا دوتریوم را جدا و خالص کنند.
جرم مولکولی آب معمولی ١٨ و جرم مولکولی آب سنگین ٢٠ است. از لحاظ خواص شیمیایی تفاوت چندانی با خواص آب معمولی نداشته و اختلافات جزئی وجود دارد اما از لحاظ هسته ای هیدروژن معمولی می تواند نوترون را جذب کند اما احتمال جذب نوترون توسط هیدروژن سنگین بسیار کم است. چنانچه بخواهیم یک راکتور هسته ای بسازیم که با آب خنک شود چون هیدروژن آب جاذب نوترون است، مجبوریم که اورانیوم غنی شده به کار ببریم، اما اگر از آب سنگین استفاده کنیم می توانیم برای نیروگاه هسته ای از اورانیوم طبیعی استفاده کنیم.
به دلیل تفاوت مشخصات هسته ای دوتریوم با هیدروژن از لحاظ تکانه زاویه ای و گشتاور مغناطیسی از آب سنگین و دوتریوم در زمینه های مختلف تحقیقاتی نیز استفاده می شود. به عنوان مثال رفتار آب سنگین در دستگاه های MRIبا رفتار هیدروژن معمولی متفاوت است. در فعالیت های تحقیقاتی به منظور بررسی برخی خواص از موادی استفاده می کنند که هیدروژن طبیعی را در آن با هیدروژن سنگین (دوتریوم)جایگزین کرده اند. یکی از کاربردهای دوتریوم استفاده در تولید نوترون در شتاب دهنده ها و تولید انرژی در «راکتورهای گداخت» است.
فشرده اطلاعات آب سنگین1 - دوتریوم برای تولید تریتیم و کلاهک بمب هسته ای از اجزای اساسی به شمار می رود.
2- آب سنگین برای تعدیل نوترونی راکتورهای هسته ای با هدف آهسته کردن حرکت نوترون ها برای واکنش با اورانیوم طبیعی و تولید پلوتونیم به کار می رود.
3 - آب سنگین به طور طبیعی به میزان ناچیزی با نسبت ١ به ۵٠٠٠ در آب معمولی وجود دارد.
4 - از مزایای استفاده از آب سنگین حذف مراحل غنی سازی اورانیوم برای تولید پلوتونیم برای استفاده در سلاح های هسته ای است. راکتورهای آب سنگین برای تولید تریتیم می توانند به کار روند.
5- آب سنگین برای تعدیل سازی نوترونی راکتورهای آب سنگین به کار می رود.
برخی از خواص آب معمولی و آب سنگین
H2O
D2O
ویژگی
0.0 (°C)
3.82
نقطه ذوب
100 (°C)
101.4
نقطه جوش
0.9982
1.1056
چگالی درat 20°C, g/mL
4.0
11.6
درجه حرارت بالترین چگالی (°C)
1.005
1.25
(at 20°C, centipoise)ویزکوزیتی
71.97
71.93
(at 25°C, dyn·cm) کشش سطحی
1,436
1,515
(cal/mol)حرارت ترکیب
10,515
10,864
حرارت بخار (cal/mol)
7.00
7.41
pH -at 25°C
چون چگالی آب سنگین از آب معمولی بیشتر است، یخ تولید شده از آب معمولی که روی آب شناور است در حالیکه یخ تولید شده از آب سنگین در آب غوطه ور است.
آب نیمه سنگین
چنانچه در اکسید هیدروژن تنها یکی از اتمهای هیدروژن به یزوتوپ دوتریوم تبدیل شود نتیجه حاصله (HDO) را آب نیمه سنگین می گویند. در مواردی که ترکیب مساوی از هیدروژن و دوتریوم در تشکیل مولکوهی آب حضور داشته باشند، آب نیمه سنگین تهیه می شود. دلیل ین امر تبدیل سریع اتم هی هیدروژن و دوتریوم بین مولکولهی آب است، مولکول آبی که از 50 درصد هیدروژن معمولی (H) و 50 درصد هیدروژن سنگین(D) تشکیل شده است، در موازنه شیمیایی در حدود 50 درصد HDO و 25 درصد آب (H2O) و 25 درصد D2O خواهد داشت.
نکته قابل توجه آن است که آب سنگین را نباید با با آب سخت که اغلب شامل املاح زیاد است و یا یا آب تریتیوم (T2O or 3H2O) که از یزوتوپ دیگر هیدروژن تشکیل شده است، اشتباه گرفت. تریتیوم ایزوتوپ دیگری از هیدروژن است که خاصیت رادیواکتیو دارد و بیشتر بری ساخت موادی که از خود نور منتشر می کنند بکار برده می شود.
آب با اکسیژن سنگین
آب با اکسیژن سنگین، در حالت معمول H218O است که به صورت تجارتی در دسترس است ببیشتر بری ردیابی بکار برده می شود. بعنوان مثال با جایگزین کردن این آب (از طریق نوشیدن یا تزریق) در یکی از عضوهای بدن می توان در طول زمان میزان تغییر در مقدار آب این عضو را بررسی کرد.
ین نوع از آب به ندرت حاوی دوتریوم است و به همین علت خواص شیمیایی و بیولوژیکی خاصی ندارد بری همین به آن آب سنگین گفته نمی شود. ممکن است اکسیژن در آنها بصورت ایزوتوپهای O17 نیز موجود باشد، در هر صورت تفاوت فیزیکی ین آب با آب معمولی تنها چگالی بیشتر آن است.
| | نسخه قابل چاپ | تعداد بازديد : 209 |
اتم هیدروژن در واقع حالت مقید یک الکترون و یک پروتون است. هسته اتمی عناصر دیگر از پروتونها و نوترونهایی تشکیل میشود که با برهمکنشی قوی در قید یکدیگرند. پروتونهای آزاد را میتوان هم در پرتوهای کیهانی یافت و هم با شتاب دهندههای ذرات تولید کرد. در آزمایشهای ویلهلم وین در سال 1898 و آزمایشهای متأخر جوزف تامسون در سال 1910، در میان ذرات یافت شده در جریانهای گازی یونیده ، ذره آلی با بار مثبت شناسایی شد که جرم آن تقریبا با جرم اتم هیدروژن بود.
در سال 1911 ارنست رادرفورد، در آزمایشهایی که در آنها که نیتروژن با ذرات آلفا بمباران می شد، دوباره با چنین ذرات باردار مثبتی روبرو شد و آنرا به عنوان هسته هیدروژن شناسایی کرد. تا سال 1920، او به این نتیجه رسیده بود که این ذره ، ذره بنیادی است و با توجه به این که واژه "protos" ، در زبان یونانی به معنی نخستین است، آنرا پروتون نامید تا موقعیت اولیه در خور اهمیت آن را در میان هستههای اتمی عناصر نشان دهد.

جرم پروتون برابر است با mp = 938.272 MeV/C2 = 1.6726X10-27 Kg جرم پروتون 1836 برابر جرم الکترون است. برای مشاهده واپاشی پروتون به ذرات سبکتر ، جستجوی تجربی فراوانی انجام شده ، ولی تا به حال نتیجهای حاصل نشده است. مستقل از مد واپاشی ، حد پایین طول عمر میانگین پروتون ، τ ، را می توان حدود 1025 سال دانست. عمر میانگین پروتون در بعضی از مدهای واپاشی خاص به حد بالاتری میرسد، برای مثال در واپاشی p → e+ + π0 مقدار τ بزرگتر از 1032 سال است.
بار الکتریکیبار الکتریکی پروتون مثبت است. این بار در مقایسه با بار الکترون مقداری مساوی و علامتی مخالف دارد. qp = -qe = -e شواهد تجربی نشان میدهد که ماده (از لحاظ بار الکتریبکی) خمثی است و در آن lim (|qp + qe|/e)<1021 است. حد گشت و در دو قطبی الکتریکی پروتون ، dp ، کمتر از 7-10 emf است (1fm = 10-15m) ، و میانگین مربعی شعاع بار پروتون که در آزمایشهای پراکندگی الکترون از پروتون بدست میآید، در حدود 0.72fm2 است. پروتون دارای تکانه زوایه ای h/2 ، پاریته مثبت و گشتاور مغناطیسی 2.792847µN است (µN مگنتون هستهای است).
نوترون ذرهای است که ساختارش شباهتهای فراوانی به ساختار پروتون دارد. تشابه جرم پروتونم و نوترونها ، در کنار یکسان بودن تکانه زاویهای (اسپین) هر ذره یکسانی تقریبی برهمکنشی قوی میان پروتونها و برهمکنش قوی میان نوترونها ، به معنی مفهوم ایزوسپین منجر میشود. پروتون و نوترون را مشترکا نوکلئون مینامند. نوکلئون به دسته ذراتی که باریون نامیده میشود تعلق دارد. باریون تکانه زاویهای نیمه صحیح (با یکای h) دارد. نوکلئون سبکترین باریون است.
پروتون پاد ذرهای به نام پاد پروتون دارد. پاد پروتون را اوئن چمبرلین ، امیلیو سگره ، کلاید ویگاند و توماس یسپسیلانتیس در سال 1955 میلادی ، با استفاده از بواترون در آزمایشگاه تابش برکلی ، کشف کردند. پس از مدت زمان کوتاهی ، پاد نوترون نیز با استفاده از همین بواترون کشف شد.
ترتیب در هسته اتمهسته هر اتمی از پروتونها و نوترونها (یا نوکلئونها) تشکیل میشود. و این نوکلئونها از طریق برهمکنش قوی با یکدیگر پیوند دارند. ترکیب پروتونها و نوترونها در هر هسته معین بصورت A Z نشان داده نی شود که در آن ، A = Z+N است ، N و Z به ترتیب تعداد نوترونها و تعداد پروتونها است. تعداد پروتونها در هسته ، تعیین کننده تعداد الکترونهای اتم و در نتیجه تعیین کننده ویژگیهای اتمی (یا شیمیایی) است. در نمایش A Z ، علامت Z را اغلب با نماد شیمیایی اتم جایگزین میکنند.
ایزوتوپهاایزوتوپها هستههایی هستند که تعداد پروتونهای آنها باهم برابر ، ولی تعداد نوترونهایشان باهم متفاوت است. برای مثال ، ایزوتوپهای پایدار کلسیوم (Z = 20) عبارتند از: 48Ca ، 46Ca ، 44Ca ، 42Ca ، 40Ca. برای پایدارترین ایزوتوپهای عناصر سبک داریم : Z < N ، که این امر به دلیل قویتربودن برهمکنش پروتون - نوترون در مقایسه با برهمکنش پروتون - پروتون و نوترون - نوترون و همچنین به دلیل این است که انرژی جنبشی برای N = Z کمینه میشود. برای عناصر سنگینتر ، تأثیر دافعه کولنی بین پروتونها بطور نسبی مهمتر میشود و در نتیجه در پایدارترین ایزوتوپ داریم: N > Z.
خواص نوکلئونها در برقراری قوانین پایستگی و تعیین دقت آنها حائز اهمیت است. پایداری پروتون ، به مفهوم باریون منجر میشود. به نوکلئون و الکترون ، به ترتیب عددهای بار Bn = 1 و Bn = 0 نسبت میدهند. قاعده پایستگی عدد بار یونی ، همراه با این واقعیت که پروتون سبکترین باریون است، مانع از واپاشی پروتون میشود. با این همه نظریه وحدت بزرگ (GUT) پیش بینی میکند که بوزونهای پیمانهای ابر سنگینی وجود دارند که در برهمکنش آنها ناپایستگی باریونها مجاز است، در نتیجه پروتون میتواند واپاشیده شود. حد تجربی طول عمر پروتون ، این مدلها را به شدت مقید میکند. برعکس الکترونها ، نوکلئونها ذرات بنیادی هستند.
برای مطالعه ساختار درونی پروتون و تولید ذرات جدید ، پروتون را تا انرژی حدود 106 Mev (معادل 1TeV) شتاب میدهند تا با الکترونها ، پروتونها یا هستهها برخورد کند. پروتونهای شتابدار ، یا مستقیما از طریق نوترونهایی که در واکنشهای بعدی تولید میشوند. برای نابود کردن بافتهای سرطانی نیز مورد استفاده قرار میگیرند. پروتونها ، بخش اصلی پروتونهای کیهانی را تشکیل میدهند. پروتونهای با انرژی بسیار زیاد ، وقتی که وارد لایه بالایی جو میشوند، سرانجام در برخورد با هستهها ، رگباری ذرهای پدید میآورند که چون به زمین میرسند بطور تجربی قابل آشکار سازی هستند.
پروتون (Proton) ذرهای بنیادی با بار مثبت است که بخشی از هر اتم را تشکیل میدهد. جرم پروتون ۱۸۳۷ برابر جرم الکترون، و معادل ۱ amu است.
بر اساس قوانین پایستگی و به علت آنکه پروتون سبکترین باریون است پایدار است اما براساس نظریه وحدت بزرگ این ذره عمر ۱.۶×۱۰۳۰ سال داشته و بعد از این مدت به پوزیترون و پیون صفر تبدیل میشود.[۱]
| | نسخه قابل چاپ | تعداد بازديد : 43 |
تشابه بین آذرخش و جرقه الکتریکی در همان اوایل قرن هجدهم مورد توجه قرار گرفت. تصور میشد که ابری طوفانی بار الکتریکی زیادی حمل میکنند، و آذرخش جرقه غول آسایی است که فقط از نظر اندازه با جرقه بین الکترودهای ماشین ویمچورست متفاوت است. این مطلب را مثلاً لومونوسوف (M. V. Lomonosov) فیزیکدان و شیمیدان روسی که الکتریسته جو را همراه با مسائل علمی دیگر مطالعه کرد، خاطر نشان نمود. این مطلب با آزمایشهایی که لومونوسوف در سالهای 1752 و 1753 و فرانکلین (B. Franklin) پژوهشگر آمریکایی بطور مستقل انجام دادند، تأیید شده است.
ماشین تندر لومونوسوفلومونوسوف یک ماشین تندر ساخت. خازنی که در آزمایشگاه او نصب شده بود و با سیمی که انتهایش از اتاق خارج و بر تیرک بلند بالا برده شده بود، با الکتریسته جو باردار می شد. در مدت طوفانهای تندری ، با لمس کردن خازن می شد جرقه را از آن خارج کرد.
آزمایش فرانکلینفرانکلین در مواقع طوفان تندری بادبادکی را با یک میله آهنی به هوا فرستاد. انتهای پایین ریسمانی که به بادبادک متصل بود به کلید دری بسته میشد. وقتی که ریسمان مرطوب و به رسانای الکتریکی تبدیل میشد، فرانکلین میتوانست جرقهها را از کلید بگیرد، بطری لید را پرکند. و سایر آزمایشهایی را که معمولاً با ماشین ویمچورست صورت میپذیرفت، انجام دهد.
باید خاطرنشان کرد که چنین آزمایشاتی بسیار خطرناکند زیرا آذرخش ممکن است به بادبادک بخورد و آن وقت بار زیادی از بدن آزمایشگر به زمین برسد (برق گرفتگی شدید). در تاریخ فیزیک چنین موارد دردناکی وجود دارند. مثلاً در سال 1753ریچمن (G. Richman) که با لومونوسوف کار میکرد در سن پترزبورک توسط آذرخش کشته شد.

قسمتهای مختلف ابر بارهایی با علامتهای مختلف حمل میکنند. در بیشترین موارد پایین ابر (که به زمین است) دارای بار منفی است. در حالیکه قسمت بالا بطور مثبت باردار است. بنابراین اگر دو ابر چنان بهم نزدیک شوند که قسمتهایی که بار غیر همنام دارند، به طرف یکدیگر باشند، ممکن است بین آنها جرقه آسمانی (آذرخش) بوجود آید.
همچنین تخلیه آذرخش ممکن است به طریقه دیگری نیز صورت گیرد، ابر طوفانی با حرکت در بالای زمین بار زیادی بر سطح زمین القا میکند و ابر سطح زمین بصورت صفحات خازنی بزرگی در میآیند. اختلاف پتاسیل الکتریکی بین ابر و زمین به مقادیر عظیم صدها میلیون ولت می رسد و میدان الکتریکی شدیدی در هوا به وجود میآید. اگر شدت این میدان به قدر کافی زیاد باشد، ممکن است جرقه زنی روی دهد یعنی آذرخش به زمین بربخورد. گاهی آذرخشها به زمین میخورند یا باعث آتش سوزی میشوند.
پارامترهای مشخص کننده آذرخش
بنا بر مشاهدات دراز مدت تخلیه الکتریکی آذرخش با عوامل زیر مشخص میشود.
ولتاژ بین ابر و زمین که حدودا 108 ولت است. جریان در آذرخش که حدودا 105 آمپر است. مدت آذرخش که حدودا 6-10 ثانیه است. قطر کانال تابان آذرخش که حدودا 10 تا 20 سانتیمتر است. تندر آذرخشتندر که بعد از آذرخش شنیده میشود، دارای همان منشأ ترق ترقی است که در مدت جرقه در آزمایشگاه بوجود میآید. یعنی هوای درون کانال تابان آذرخش به شدت گرم و منبسط می شود و موجهای صوتی ایجاد میکند. در نتیجه بازتاب از ابرها ، کوه ها و غیره پژواک غرشهای تندر را اغلب میتوان شنید.
فواید و برکات رعد و برق آبیاریبرقها معمولا حرارت فوق العاده زیاد گاه در حدود 15 هزار درجه سانتیگراد تولید میکنند و این حرارت کافی است که مقدار زیادی از هوای اطراف را بسوزاند و در نتیجه فشار هوا فورا کم شود و میدانیم در فشار کم ، ابرها میبارند و به همین دلیل غالبا بعد از جهش برق رگبارهایی شروع میشود و دانههای درشت باران فرو می ریزند. از اینرو برق در واقع یکی از وظایفش آبیاری است.
سمپاشیهنگامی که برق با آن حرارتش آشکار میشود، قطرات باران با مقداری اکسیژن اضافی ترکیب میشوند و آب سنگین یعنی آب اکسیژنه ایجاد میکنند و هنگام بارش تخم آفت و بیماریهای گیاهی را از میان میبرد و در واقع عمل سمپاشی انجام میدهد. هر سال که رعد و رق کم باشد آفات گیاهی بیشتر است!
تغذیه و کود رسانیقطرات باران بر اثر برق و حرارت شدید ، ترکیب اسید کربنی پیدا میکنند و به هنگام پاشیده شدن بر زمین و ترکیب با آن یک نوع کود مؤثر گیاهی میسازند و گیاهان از این طریق تغذیه میشوند. بعضی از دانشمندان گفتهاند مقدار کودی که در یک سال از مجموع برقهای آسمان در کره زمین بوجود میآید دهها میلیون تن است، که رقم فوق العاده بالایی میباشد.
منبع: سایت رشد
| | نسخه قابل چاپ | تعداد بازديد : 38 |
فیزیک ذرات بنیادی چیست؟
فیزیک ذرات بنیادی بخشی از فیزیک است. موضوع مورد مطالعه ی فیزیکدانان ذرات بنیادی این است. که بدانند جهان از چه ذراتی ساخته شده و این ذرات چگونه در کنش با یکدیگر هستند. اما این ذرات چه هستند؟
در حدود سال 1900
تصور می شد که اتم سنگ بنای جهان است و غیر قابل تجزیه می باشد .
بزودی مشخص شد که
اتم از یک هسته ی مرکزی با الکتریکی مثبت وتعدادی الکترون که در اطراف آن در گردشند، تشکیل شده است.
هنگامیه هسته مورد مطالعه قرار گرفت، فیزیکدانان متوجه شدندکه هسته از پروتون با بار الکتریکی مثبت و نوترون که از نظر الکتریکی حنثی است تشکیل شده و الکترونها در اطراف آن در گردشند.
ماده از چه ذراتی ساخته شده است؟
هرچه تحقیقات روی هسته بیشتر انجام می شد، ذرات جدیدی کشف می شدند. همچنین تحقیقات بیشتر نشان دادکه پروتونها و نوترونها نیز از ذرات دیگری که کوارک نامیده شدند ساخته شده است سرانجام فیزیکدانان ذرات سازنده ی ماده را به دو دسته: لپتونها و کوارکها تقسیم کردند. در این تقسیم بندی هادرونهااز جمله پروتون و نوترون ذره ی بنیادی نیستندو از کوارکها ساخته شده اند.
پاد ماده
یکی از کشفیات بسیار جالب، کشف پاد ماده است برای هر ذره ی بنیادی یک ذره دیگری وجود دارد که آن را پا ماده ی آن می نامند. به عنوان مثال پاد ماده ی الکترون، پوزیترون است که تنها از نظر الکتریکی با هم تفاوت دارند. ماده و پاد ماده یکدیگر را جذب کرده و به انرژی تبدیل می شوندبهمین دلیل آنها را پاد ماده می نامند,
توجه شود که پاد ماده تنها یک اصطلاح است و از نظر فیزیکی هر دوی آنها ماده می باشند.
اسپین
اسپین یکی از خواص ذرات مانند جرم و بار است. اسپین اندازه ی حرکت زاویه ای ذره استو ساده ترین راه برای اندازه گیری اندازه حرکت زاویه ای ذره بر اثر گردش آن است. در واقع سخن از گردش ذره درست نیست، بلکه اندازه حرکت زاویه ای ذره یکی از خواص ذاتی ذرات است. اسپین نظیر اندازه حرکت و انرژی در تمام مراحل ثابت است
کوارکها
شش کوارک و شش پاد کوارک وجود دارد که که سه دسته دوتایی تشکیل می دهند. این گروهها عبارتند از:
up-down
بالا-پایین
charm-strange
عجیب-افسون
top-bottom
سر- ته
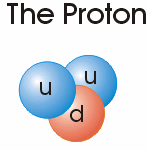
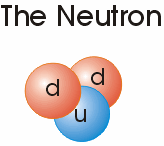
یک خاصیت دیگر جالب کوارکها این است که هیچگاه کوارکها به تنهایی مشاهده نمی شوندو آنها در کنار یکدیگر قرار دارند و ذرات مرکب را می سازند. این ذرات مرکب هادرون نامیده می شوند. کوارکها نطیر الکترون و پروتون دارای بار الکتریکی هستند. اما بار الکتریکی کوارکها کسری از بار الکتریکی پایه است.
Flavour
Mass
(GeV/c2)
Electric Charge
(e)
u
up
0.004
+2/3
d
down
0.08
-1/3
c
charm
1.5
+2/3
s
strange
0.15
-1/3
t
top
176
+2/3
b
bottom
4.7
-1/3



Leptons
Flavour
Mass
(GeV/c2)
Electric Charge
(e)
electron neutrino
-9
0
electron
0.000511
-1
muon neutrino
0
muon
(mu-minus)
0.106
-1
tau neutrino
0
tau
(tau-minus)
1.7771
-1
نیروها
نیروهای اساسی طبیعت عبارتند از:
نیروی الکترومغناطیسی
هسته ای ضعیف
هسته ای قوی
گرانش

همه ی این نیروها توسط ذرات تبادلی حمل می شوند
به عنوان مثال ذرات تبادلی نیروی الکترومغناطیسی فوتون نامیده می شود. الکترون و پروتون با انتشار و جذب فوتون همدیگر را جذب می کنند
همچنین نوترینو یک ذره بدون بار الکتریکی است، بنابراین فوتون منتشر یا جذب نمیکند.
نیروی هسته ای ضعیف
همه ی اجسام پایدار موجود در جهان از یک نوع لپتون (الکترون) و دو کوارک (بالا-پایین) ساخته شده اند که ترکیب این دو کوارک بصورت پروتون و نوترون ظاهر می شود. در هر صورت شش تای آنها پیشگویی و مشاهده شده اند و شش تای دیگر مشاهده نشده اند، زیرا:
کوارکها و لپتونهای سنگین به دلیل وجود نیروی هسته ای ضعیف قابل مشاهده نمی باشند.
نیروی هسته ای ضعیف باعث می شود که کوارکها و لپتونهای سنگین به کوارکها و لپتونهای سبکتر واپاشیده شوند.
ذره ی حامل نیروی واپاشی لپتونها و کوارکهای سنگین
W and +W-
هر کدام از اینها شامل یک ذره ی باردار و یک ذره ی خنثای Zاست
علاوه بر بار الکتریکی، کوارکها دارای خاصیت دیگری هستند که بار - رنگ نامیده می شود colour charge

نیروی بین درات بار - رنگ بسیار قوی است که آنرا نیروی قوی می نامند.
نیروی قوی بسیار سخت و جاذبه است که روی پروتونها و نوترونها اعمال می شود
این نیرو بر نیروی دافعه الکتریکی بین پروتونها غلبه می کند و موجب می شود هسته پایدار بماند.
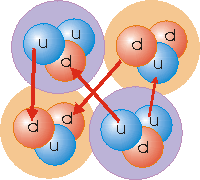
در واقع نیروی قوی بین کوارکها اعمال می شود
ذره ای که این نیرو را حمل می کندگلوئونgluon
نامیده می شود
مدل استاندارد ذرات بنیادی
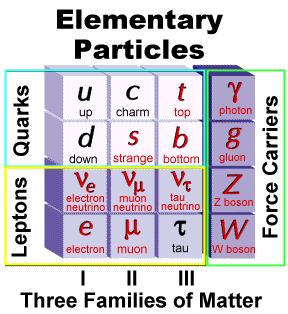
با توجه به مطالب بالا مدل استاندارد ذرات بنیادی به شرح زیر است
شش عدد کوارک
شش عدد لپتون
و چهار بوزون که نیروها را حمل می کنند
بطور کلی ذراتی که ماده را می سازند فرمیون
و ذراتی که نیرو ها را حمل می کنند بوزون
نامیده می شوند
منبع: سایت سی پی اچ
ادامه مطلب...
| | نسخه قابل چاپ | تعداد بازديد : 212 |
 |
|